
����Ŀ��ijУ��ѧ�о���ѧϰС����������˽�������ݣ�
�Ҷ��ᣨHOOC��COOH���ɼ�дΪH2C2O4���׳Ʋ��ᣬ������ˮ�����ڶ�Ԫ��ǿ�ᣨΪ������ʣ���������ǿ��̼�ᣬ���۵�Ϊ101.5�棬��157��������Ϊ̽������IJ��ֻ�ѧ���ʣ�����������ʵ�飺
��1����ʢ��1mL����NaHCO3��Һ���Թ��м��������Ҷ�����Һ���۲쵽����ɫ���ݲ������÷�Ӧ�����ӷ���ʽΪ________��
��2����ʢ���Ҷ��ᱥ����Һ���Թ��е��뼸�������ữ��KMnO4��Һ������������Һ���Ϻ�ɫ��ȥ����˵���Ҷ������______��������������������ԭ������������������������ƽ�÷�Ӧ�����ӷ���ʽ��_____MnO4-+____H2C2O4+___H+=___Mn2++____CO2��+_____H2O
��3����һ�������Ҷ�������Թ��У�����ͼ��ʾװ�ý���ʵ�飨�г�װ��δ�������

ʵ�鷢�֣�װ��C��G�г���ʯ��ˮ����ǣ�B��CuSO4��ĩ������F��CuO��ĩ��졣�ݴ˻ش�
������װ���У�D��������_________��
���Ҷ���ֽ�Ļ�ѧ����ʽΪ ________��
��4����С��ͬѧ��2.52g���ᾧ�壨H2C2O42H2O�����뵽100mL 0.2mol/L��NaOH��Һ�г�ַ�Ӧ����÷�Ӧ����Һ�����ԣ���ԭ����_______�������ּ�����������Һ�и����ӵ�Ũ���ɴ�С��˳��Ϊ��_______�������ӷ��ű�ʾ����
���𰸡�HCO3-+H2C2O4=HC2O4-+CO2��+H2O ��ԭ�� 2 5 6 2 10 8 ��ȥ��������е�CO2 H2C2O4![]() H2O+CO��+CO2�� ��Ӧ������ҺΪNaHC2O4��Һ������HC2O4���ĵ���̶ȱ�ˮ��̶ȴ�����Һ��c��H+����c��OH������������Һ������ Na+��HC2O4-��H+��C2O42-��OH��
H2O+CO��+CO2�� ��Ӧ������ҺΪNaHC2O4��Һ������HC2O4���ĵ���̶ȱ�ˮ��̶ȴ�����Һ��c��H+����c��OH������������Һ������ Na+��HC2O4-��H+��C2O42-��OH��
��������
��1��ǿ��������ԭ����
��2�����Ը�����ؾ���ǿ�����ԣ�������л�ԭ�ԣ��ܱ����Ը���������������ݵ�ʧ�����غ�͵���غ���ƽ���ӷ���ʽ��
��3��H2C2O4![]() H2O+CO��+CO2����Bװ����֤����ˮ��Cװ����֤����CO2��Dװ�ó���CO2��Eװ�ó���ˮ������F��Gװ����֤����CO���ݴ˷�����
H2O+CO��+CO2����Bװ����֤����ˮ��Cװ����֤����CO2��Dװ�ó���CO2��Eװ�ó���ˮ������F��Gװ����֤����CO���ݴ˷�����
��4��ͨ�����㷴Ӧ����ҺΪNaHC2O4��Һ�����ݷ�Ӧ����Һ�����ԣ���֪HC2O4- �ĵ���̶ȱ�ˮ��̶ȴ��ɴ�ȷ����Һ�и�����Ũ�ȵ���С��
��1���Ҷ����к����Ȼ����������ԣ����Ա�̼��ǿ����̼�����Ʒ�Ӧ���ɶ�����̼�������ƣ��÷�Ӧ�����ӷ���ʽΪ��HCO3-+H2C2O4=HC2O4-+CO2��+H2O��
�𰸣�HCO3-+H2C2O4=HC2O4-+CO2��+H2O��
��2������KMnO 4 ��Һ����ǿ�����ԣ���ʢ�������Ҷ��ᱥ����Һ���Թ��е����������ữ��KMnO 4��Һ������������Һ���Ϻ�ɫ��ȥ��˵���Ҷ��ᱻ���Ը���������������л�ԭ�ԣ�����������ԭ��Ӧ����ʽ����ƽԭ��ʧ�����غ㡢�����غ�͵���غ���ƽ�÷�Ӧ�����ӷ���ʽ��2MnO 4 - +5 H2C2O4 +6H + =2Mn 2+ +10CO 2 ��+8H2O��
�𰸣���ԭ�� 2 5 6 2 10 8
��3�������Ҷ��ᣬ��Ӧ��ͨ��B��ʹCuSO 4 ��ĩ������˵����ˮ���ɣ�װ��C�г���ʯ��ˮ����ǣ�˵���ж�����̼���ɣ�װ��D�ж�����̼���������Ʒ�Ӧ��ȥ��������еĶ�����̼��F��CuO��ĩ��졢G�г���ʯ��ˮ�����˵����һ����̼���ɣ������Ҷ���ķֽ����ΪCO��CO 2 ��H2O��
�𰸣���ȥ��������е�CO2�� H2C2O4![]() H2O+CO��+CO2����
H2O+CO��+CO2����
��4����2.52g���ᾧ������ʵ���= ![]() =0.02mol��100mL 0.2mol/L��NaOH��Һ���������Ƶ����ʵ���=100mL��10 -3 L/mL��0.2mol/L=0.02mol�����Է�Ӧ����NaHC2O4 ��������ҺΪNaHC2O4��Һ������HC2O4 - �ĵ���̶ȱ�ˮ��̶ȴ�����Һ��c��H + ����c��OH - ����������Һ�����ԣ�
=0.02mol��100mL 0.2mol/L��NaOH��Һ���������Ƶ����ʵ���=100mL��10 -3 L/mL��0.2mol/L=0.02mol�����Է�Ӧ����NaHC2O4 ��������ҺΪNaHC2O4��Һ������HC2O4 - �ĵ���̶ȱ�ˮ��̶ȴ�����Һ��c��H + ����c��OH - ����������Һ�����ԣ�
����������1��1��Ӧ����NaHC2O4����Һ�����ԣ�˵��HC2O4 - �ĵ���̶ȱ�ˮ��̶ȴ���Һ�л�������ˮ�ĵ��룬��H+��C2O42-���������ӵĵ���̶Ƚ�С������HC2O4-��H+������Ũ���ɴ�С��˳��ΪNa+��HC2O4-��H+��C2O42-��OH����
�𰸣���Ӧ������ҺΪNaHC2O4��Һ������HC2O4���ĵ���̶ȱ�ˮ��̶ȴ�����Һ��c��H+����c��OH������������Һ������ Na+��HC2O4-��H+��C2O42-��OH��


 100�ִ�����ĩ���ϵ�д�
100�ִ�����ĩ���ϵ�д� ��У���˿��ֿ���ϵ�д�
��У���˿��ֿ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��Q��R��T��W��Ԫ�����ڱ��е�λ����ͼ��ʾ������T��������������������������ȣ����������������

A. T������������Ӧ
B. Ԫ�صķǽ����ԣ�Qǿ��W
C. W�ĵ��ʹ���ʱ������������������ˮ����Ũ��Һ��Ӧ
D. ԭ��������R��1��Ԫ�ص�һ���⻯���ֽܷ�Ϊ������һ���⻯��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С�������ð�����CuO��Ӧ,�о����������ʲ��������,���������ʵ�飨�г�װ��δ����������ʵ�顣��ش��������⣺

��1������a������Ϊ____________������b�п�ѡ����Լ�Ϊ��������һ�֣�_____________��
��2��ʵ���У�װ��C�к�ɫCuO��ĩȫ��ת��Ϊ��ɫ���壨��֪Cu2OҲΪ��ɫ���壩��������������ɫ��ζ�����塣ʵ��ǰ��ȡ��ɫCuO 80g��ʵ���õ���ɫ��������Ϊ68g�����ɫ����ɷֵĻ�ѧʽΪ_______________��
��3��Eװ����Ũ�����������____________________________________��
��4��F�ж�ȡ�������ǰ��Ӧ��װ��F���еIJ����ǣ�___________________�����˲�������F�����Һ������ұ�Һ�棬�ᵼ�¶�ȡ���������________ ���ƫ��ƫС������Ӱ�족����ͼ�������ܿ���________ ����ѡ����ĸ��գ�A����ʽ�ζ��ܣ�B����ʽ�ζ��ܣ���װ���ɡ�
��5��Ҫ���ð��������е�����ԭ�Ӹ����ȣ�ʵ����Ӧ���ٲ������ȡ��Щ����________��
A��Bװ��ʵ��ǰ��������mg�� B��Fװ��ʵ��ǰ��Һ���VL
C��Dװ��ʵ��ǰ��������mg�� D��Eװ��ʵ��ǰ��������mg��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�á���ͼ��ʾһ�����أ� װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺
����8�֣���X��Y���Ƕ��Ե缫��a�DZ���NaCl��Һ��ʵ�鿪ʼʱ��ͬʱ�����߸����뼸�η�̪��Һ����
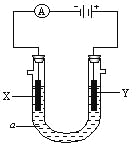
��������X���ϵĵ缫��Ӧʽ�� ��
��X�������۲쵽�������� ��
��Y�缫�ϵĵ缫��Ӧʽ�� ��
����õ缫��Ӧ����ķ����� ��
����6�֣���Ҫ�õ�ⷽ��������ͭ�����Һaѡ��CuSO4��Һ����
��X�缫�IJ����� ���缫��Ӧʽ��
��Y�缫�IJ����� ���缫��Ӧʽ��
��˵�������ʷ����ĵ缫��Ӧ����д����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Խ�����Ʒ���и㸯ʴ���������ӳ���ʹ��������
��1������Ϊ������洦����һ�ַ�����

����ϴ��Ŀ���dz�ȥ����������Ȼ����Ĥ����ϴ��ʱ��������ð����ԭ���ǣ�________�������ӷ���ʽ��ʾ����Ϊ����ϴ��Һ�е����Գ�����ʽ���գ�������Һ�м��������Լ��е�__________��
a.NH3b.CO2c.NaOH d.HNO3
��������Ϊ��������H2SO4��Һ�е�⣬��������γ�����Ĥ�������缫��ӦʽΪ��_____��
ȡ�����ϵ��Һ������NaHCO3��Һ��������ݺͰ�ɫ����������������ԭ����_________��
(2)��ͭ�ɷ�ֹ����Ʒ��ʴ�����ʱ��ͭ������ʯī��������ԭ���� ��
��3��������ͼװ�ã�����ģ�����ĵ绯ѧ������

��XΪ̼����Ϊ�������ĸ�ʴ������KӦ������ ����
��XΪп������K����M�����õ绯ѧ��������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����mgͭ˿���ձ�ڣ������������������У���ʹͭ˿������������Ϊmg����( )
A. NaOH��Һ B. CH3COOH C. ϡHNO3 D. CH3CH2OH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ӧ�ù㷺�Ľ�������������(��Ҫ�ɷ�ΪAl2O3����SiO2��Fe2O3������)Ϊԭ���Ʊ�����һ�ֹ����������£�

ע��SiO2����������ʱת��Ϊ�������Ƴ�����
��1����������ʱ����ƫ�����Ƶ����ӷ���ʽΪ_____________________��
��2������������������Һ�м���NaHCO3��Һ����Һ��pH_________ (��������������������������С��)��
��3����������ǵ������Al2O3������������������ʯī�����ģ�ԭ����___________��
��4����������ǵ��Na2CO3��Һ��ԭ����ͼ��ʾ�������ĵ缫��ӦʽΪ_____________________����������������A�Ļ�ѧʽΪ____________��
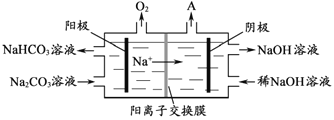
��5��������1000��ʱ����N2��Ӧ�Ʊ�AlN������������������NH4Cl���岢��ֻ�ϣ�������AlN���Ʊ�������Ҫԭ����_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йص������Һ��˵����ȷ����![]() ����
����![]()
A. ��![]() ��Һ�м�������ˮ����Һ��
��Һ�м�������ˮ����Һ��![]() ��С
��С
B. ��![]() ��Һ��
��Һ��![]() ������
������![]() ����Һ��
����Һ��![]() ����
����
C. �������м��백ˮ�����ԣ���Һ��![]()
D. ��AgCl��AgBr�ı�����Һ�м�������![]() ����Һ��
����Һ��![]() ����
����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��ӦA��g����3B��g��![]() 2C��g����2D��g�����������ĸ�ѡ�����Dz�ͬ������²�õIJ�ͬ���ʵķ�Ӧ���ʣ����б�ʾ�û�ѧ��Ӧ�ķ�Ӧ����������
2C��g����2D��g�����������ĸ�ѡ�����Dz�ͬ������²�õIJ�ͬ���ʵķ�Ӧ���ʣ����б�ʾ�û�ѧ��Ӧ�ķ�Ӧ����������
A.����A����0.2mol(L��min)B.����B����0.45 mol(L��s)
C.����C����0.40 mol(L��min)D.����D����0.35 mol(L��min)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com