
| A、7.1gCl2与5.6gFe反应,转移的电子总数为0.3NA |
| B、实验室中用含4molHCl的浓盐酸跟足量MnO2加热反应可制得Cl2的分子数为NA |
| C、1 mol OH-和1 mol-OH (羟基)中含有的质子数均为9NA |
| D、标准状况下,22.4mLH2O约含有 3.73NA个原子 |


科目:高中化学 来源: 题型:
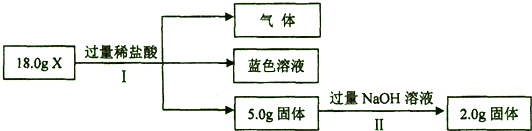
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在鸡蛋清溶液中分别加入饱和Na2SO4、CuSO4溶液,都会因盐析产生沉淀 |
| B、司母戊鼎、定远舰甲板、有机玻璃等原材料属于合金 |
| C、聚酯纤维、碳纤维、光导纤维都属于有机高分子材料 |
| D、石蜡油受热分解产生了可以使酸性高锰酸钾溶液褪色的烯烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:
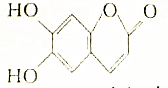 有如图所示的有机物,根据该有机物的结构回答:
有如图所示的有机物,根据该有机物的结构回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| CH4 | C2H2 | H2 | |
| 燃烧热/kJ/mo | 890.3 | 1299.6 | 285.8 |
| A、-C≡C-的键角为120° |
| B、2H2(g)+O2(g)-2H2O(g)△H=-571.6 kj?mol-l |
| C、C-H键键长小于H-H键 |
| D、2CH4(g)=C2H2(g)+3H2(g)△H=+376.4 kj?mol-l |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2:3:6 |
| B、3:2:1 |
| C、4:3:1 |
| D、6:3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com