
| 2x |
| 1-2x+0.5-x+2x |
| (2×0.25)2 |
| (1-2×0.25)2×(0.5-0.25) |
| 2y |
| n(A)-2y+n(B)-y+2y |


科目:高中化学 来源: 题型:
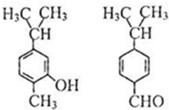
| A、不是同分异构体 |
| B、分子中共平面的碳原子数相同 |
| C、均能与溴水反应 |
| D、可用红外光谱区分,但不能用核磁共振氢谱区分 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
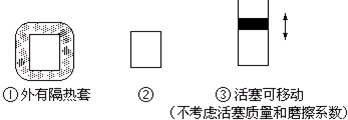
查看答案和解析>>
科目:高中化学 来源: 题型:
| 80℃,通电 |
| Ⅰ |
| 室温,KCl |
| Ⅱ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
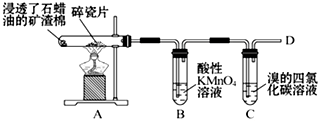 (1)如图是石蜡油在炽热碎瓷片的作用下产生乙烯并检验其性质的实验,完成下列问题.
(1)如图是石蜡油在炽热碎瓷片的作用下产生乙烯并检验其性质的实验,完成下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
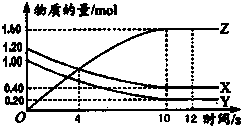
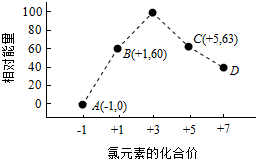
| A、反应为 X+2Z=Y |
| B、反应为 X+Y?2Z |
| C、4 s 时,反应达到平衡 |
| D、12 s 时,反应不再进行 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com