
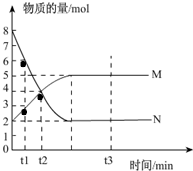
 һ���¶��£����ݻ�ΪV L���ܱ������н��з�Ӧ��aN��g��?bM��g����M��N�����ʵ�����ʱ��ı仯������ͼ��ʾ��
һ���¶��£����ݻ�ΪV L���ܱ������н��з�Ӧ��aN��g��?bM��g����M��N�����ʵ�����ʱ��ı仯������ͼ��ʾ������ ��1����ѧ����ʽ��ϵ��֮�ȵ��ڸ����ʵ����ʵ����ı仯��֮�ȣ�
��2������v=$\frac{\frac{��n}{V}}{��t}$����v��M����
��3����ͼ��֪��NΪ��Ӧ�N����ʼ���ʵ���Ϊ8mol��ƽ��ʱ�μӷ�Ӧ��N�����ʵ���Ϊ8mol-2mol=6mol���ڽ��ת���ʶ�����㣻
��4������Ӧ�ﵽƽ��״̬ʱ�������淴Ӧ������ȣ�ͬ�����ʣ��������ʵ�Ũ�ȡ��������ٸı䣬�Լ��ɴ�������һЩ������Ҳ���䣬�Դ˽����жϣ�
��� �⣺��1���μӷ�Ӧ��N�����ʵ���Ϊ8mol-2mol=6mol�����ɵ�M�����ʵ�����5mol-2mol=3mol�����Դ˷�Ӧ�Ļ�ѧ����ʽ��$\frac{a}{b}$=2��1���ʴ�Ϊ��2��1��
��2����ͼ��֪��t1��t2ʱ��M�����ʵ����仯Ϊ4mol-3mol=1mol����v��M��=$\frac{\frac{1mol}{VL}}{��{t}_{2}-{t}_{1}��min}$=$\frac{1}{{��t}_{1}-{t}_{2}����v}$mol/��L•min�����ʴ�Ϊ��$\frac{1}{{��t}_{1}-{t}_{2}����v}$mol/��L•min����
��3����ͼ��֪��NΪ��Ӧ�N����ʼ���ʵ���Ϊ8mol��ƽ��ʱ�μӷ�Ӧ��N�����ʵ���Ϊ8mol-2mol=6mol����N��ת����Ϊ$\frac{6mol}{8mol}$��100%=75%���ʴ�Ϊ��75%��
��4��A��ƽ��ʱ��Ӧ��������ֵ����ʵ������䣬������ֵ����ʵ�����һ����ȣ���A����
B����������������ʼ�ղ��䣬����������������䲻��˵������ƽ�⣬��B����
C������a��b���淴Ӧ���л�����������ʵ��������仯���������������ʵ�������ʱ��ı仯���仯��˵������ƽ�⣬��C��ȷ��
D����λʱ��������amolN��ͬʱ����bmolM������ʾ����Ӧ���ʣ���Ӧʼ�հ��˹�ϵ���У�����˵������ƽ�⣬��D����
E������a��b���淴Ӧ���л�����������ʵ��������仯����������ѹǿ����ʱ��ı仯���仯��˵����������ܵ����ʵ����ٲ��䣬˵����Ӧ����ƽ�⣬��E��ȷ��
F��N�����������ڻ�������б��ֲ��䣬˵�����淴Ӧ���������ƽ��״̬����F��ȷ��
�ʴ�Ϊ��CEF��
���� ���⿼�黯ѧ��Ӧ���ʼ��㡢��ѧƽ����㡢��ѧƽ��״̬�жϣ��ѶȲ����ضԻ���֪ʶ�Ĺ��̣�ע���жϻ�ѧƽ��״̬��������Ӧ�淴Ӧ���з����仯�����������ɱ仯�����ٱ仯˵������ƽ�⣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
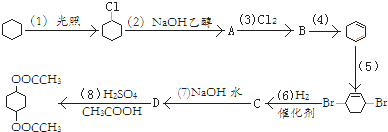
 ��ȡ����Ӧ
��ȡ����Ӧ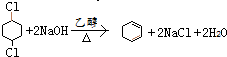 ����ȥ��Ӧ
����ȥ��Ӧ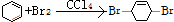 ���ӳɷ�Ӧ
���ӳɷ�Ӧ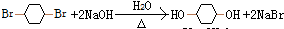 ��ȡ����Ӧ��ˮ�ⷴӦ��
��ȡ����Ӧ��ˮ�ⷴӦ��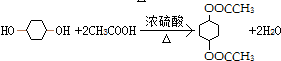 ��ȡ����Ӧ��������Ӧ����
��ȡ����Ӧ��������Ӧ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
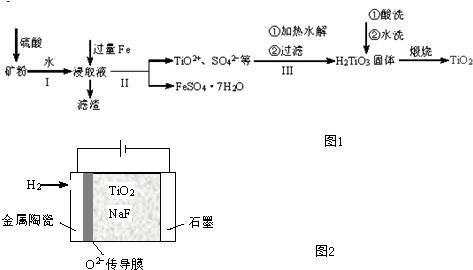
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | pH��Ϊ4��H2SO4��NH4Cl��Һ�У�ˮ�ĵ���̶���ͬ | |
| B�� | ��pH��NaOH��Һ��NH3•H2O ϡ�ͺ�pH�ı仯����ͼ��ʾ��������I��ʾ����NaOH��Һ��ϡ�� | |
| C�� | 1mol/LNa2CO3��Һ�д��ڣ�c��Na+��=2c��CO32- ��+2c��HCO3-�� | |
| D�� | ��ij�¶ȵİ�ˮ��ͨ�����ᣬ��ˮ�ĵ��볣������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | O.1molNa2O2��ˮ��Ӧת�Ƶ�����ĿΪ0.1NA | |
| B�� | ����£�2.24LCl2���µ��ӶԵ���ĿΪ0.2NA | |
| C�� | PH=2��H2SO4��Һ�к�H+����ĿΪ0.12NA | |
| D�� | ��10g��������Ϊ17%�İ�ˮ�У�����H����ĿΪ0.3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ľ�Һ���炙��ʹ�ã��൱��ʩ���˵��ͼصĸ��Ϸ��ϣ�����˷��������� | |
| B�� | �����������ܳ���ʢװ���Ի����ʳƷ���������ڳ���ʢ������ʳƷ | |
| C�� | ���ﰺ��CCl2F2����NOx�������ƻ������㣬�Ӷ������ˡ�����ЧӦ�� | |
| D�� | ����ʹ�ú���ϴ�Ӽ����ɵ���ˮ�帻Ӫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | pH=n | B�� | pH=-lg n | C�� | pH=14-lgn | D�� | pH=lgn+14 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 23g��NO2��N2O4��ɵĻ�������к��еĵ�ԭ����Ϊ0.5NA | |
| B�� | 1.12L��ϩ���뺬0.05NA������ӵ�CCl4��Һǡ����ȫ��Ӧ | |
| C�� | 1L0.1mol•L-1Fe2��SO4��3��Һ�У�Fe3+����ĿΪ0.2NA | |
| D�� | 7.8gNa2O2��ˮ��ȫ��Ӧʱת�Ƶĵ�����Ϊ0.2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com