
 有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色黏稠液体,易溶于水.为研究A的组成与结构,进行了如下实验:
有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色黏稠液体,易溶于水.为研究A的组成与结构,进行了如下实验: .
. 分析 (1)同温同压下,气体的密度之比等于相对分子质量之比,据此计算;
(2)浓硫酸增重7.2g为水的质量,碱石灰增重17.6g为二氧化碳质量,计算有机物、水、二氧化碳物质的量,进而计算n(H)、n(C),根据质量守恒确定是否含有O元素,根据元素守恒来确定有机物的分子式;
(3)能与足量的NaHCO3粉末反应,说明含有-COOH,根据生成的二氧化碳的物质的量确定-COOH数目,能与钠反应生成氢气,结合生成氢气的物质的量确定是否含有-OH及羟基数目;
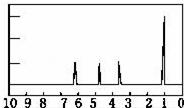
(4)核磁共振氢谱图中有几个峰值则含有几种类型的等效氢原子,峰面积之比等于氢原子的数目之比;
(5)由A的分子式、含有的官能团及核磁共振氢谱书写其结构简式.
解答 解:(1)由其密度是相同条件下H2的45倍,可知A的相对分子质量为45×2=90,摩尔质量为90g/mol,
故答案为:90g/mol;
(2)由题意可推知:n(A)=$\frac{18g}{90g/mol}$=0.2 mol,n(C)=n(CO2)=$\frac{26.4g}{44g/mol}$=0.6mol,n(H)=2n(H2O)=2×$\frac{10.8g}{18g/mol}$=1.2mol,
n(O)=$\frac{18g-0.6×12g-1.2×1g}{1g/mol}$=0.6 mol,
所以A的分子式为:C3H6O3,
故答案为:C3H6O3;
(3)0.2 mol A与NaHCO3反应放出0.2mol CO2,则说A中应含有一个羧基,而与足量金属钠反应则生成0.2 mol H2,说明A中还含有一个羟基,
故答案为:羧基、羟基;
(4)核磁共振氢谱中有4个吸收峰,面积之比为1:1:1:3,可知A中应含有4种不同环境的氢原子,
故答案为:4;
(5)综上所述,A的结构简式为: ,故答案为:
,故答案为: .
.
点评 本题考查有机物的推断,为高考常见题型,题目难度中等,侧重考查学生对知识的整合能力,注意掌握常见有机物结构与性质,根据A和碳酸氢钠、钠反应时生成气体体积判断含有的官能团类型为解答关键.


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:解答题
 .
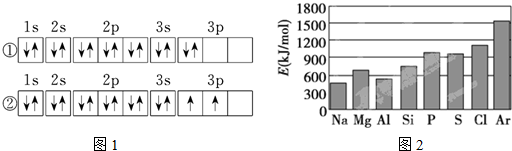
.
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
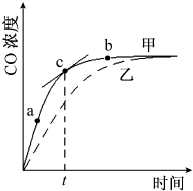 ①在温度、容积恒定的反应体系中,CO浓度随时间的变化关系如图曲线甲所示.下列说法不正确的是CD.
①在温度、容积恒定的反应体系中,CO浓度随时间的变化关系如图曲线甲所示.下列说法不正确的是CD.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量浓度之比为( )
在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量浓度之比为( )| A. | 6:1 | B. | 1:2 | C. | 2:1 | D. | 3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
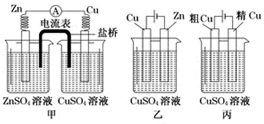
| A. | 甲是原电池,乙是电镀装置 | |
| B. | 甲、乙装置中,锌极上均发生氧化反应 | |
| C. | 乙、丙装置中,阳极均发生氧化反应而溶解 | |
| D. | 丙装置中,铜电极的质量有增有减 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 实验室中灼烧操作通常在坩埚中进行 | |
| B. | 若X为烧碱,则Z为氨气,沉淀a为红棕色,可作颜料 | |
| C. | 若X为盐酸,则Z为CO2,溶液丙只含NaCl和Na2CO3 | |
| D. | 上述过程中所发生的反应有分解反应、复分解反应、氧化还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com