
µē½āĖ®ŠĶµē½āŅ»¶ĪŹ±¼äŗó£¬Ęäµē½āÖŹµÄÅضČŅ»¶ØŌö“óĀš£æ¾ŁĄżĖµĆ÷”£

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
CuSO4ČÜŅŗÓėK2C2O4ČÜŅŗ»ģŗĻÉś³ÉŅ»ÖÖĄ¶É«¼ŲŃĪĖ®ŗĻĪļKxCuy(C2O4)z·nH2O”£ĶعżĻĀŹöŹµŃéČ·¶ØøĆ¾§ĢåµÄ×é³É”£(ŅŃÖŖ£ŗMnO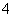 ŌŚĖįŠŌĢõ¼žĻĀ£¬¼ÓČČÄÜ·Ö½āĪŖO2£¬Ķ¬Ź±Éś³ÉMn2£«”£)
ŌŚĖįŠŌĢõ¼žĻĀ£¬¼ÓČČÄÜ·Ö½āĪŖO2£¬Ķ¬Ź±Éś³ÉMn2£«”£)
²½Öča£ŗ³ĘČ”0.672 0 gѳʷ£¬·ÅČė׶ŠĪĘ棬¼ÓČėŹŹĮæ2 mol·L£1Ļ”ĮņĖį£¬Ī¢ČČŹ¹ŃłĘ·Čܽā”£ŌŁ¼ÓČė30 mLĖ®¼ÓČČ£¬ÓĆ0.200 0 mol·L£1 KMnO4ČÜŅŗµĪ¶ØÖĮÖÕµć£¬ĻūŗÄ8.00 mL KMnO4ČÜŅŗ”£ÓŠ¹Ų·“Ó¦£ŗ2MnO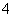 £«5C2O
£«5C2O £«16H£«===2Mn2£«£«8H2O£«10CO2”ü”£
£«16H£«===2Mn2£«£«8H2O£«10CO2”ü”£
²½Öčb£ŗ½Ó׎«ČÜŅŗ³ä·Ö¼ÓČČ”£ĄäČ“ŗ󣬵÷½ŚpH²¢¼ÓČė¹żĮæµÄKI¹ĢĢ壬ČÜŅŗ±äĪŖ×ŲÉ«²¢²śÉś°×É«³ĮµķCuI”£ÓĆ0.250 0 mol·L£1 Na2S2O3±ź×¼ČÜŅŗµĪ¶ØÖĮÖÕµć£¬ĻūŗÄ8.00 mL Na2S2O3ČÜŅŗ”£µĪ¶ØŹ±·“Ó¦ĪŖI2£«2S2O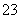 ===2I££«S4O
===2I££«S4O ”£
ӣ
(1)²½ÖčbÖŠÉś³É°×É«³ĮµķµÄĄė×Ó·½³ĢŹ½£ŗ________________________________________________________________________”£
(2)²½ÖčbÖŠ”°½«ČÜŅŗ³ä·Ö¼ÓČČ”±µÄÄæµÄŹĒ________________________________________________________________________”£
(3)ĒėĶź³ÉĻĀĮŠČ·¶Øѳʷ×é³ÉµÄ¼ĘĖć¹ż³Ģ”£
¢Ł¼ĘĖćѳʷ֊n(C2O )(Š“³ö¼ĘĖć¹ż³Ģ)
)(Š“³ö¼ĘĖć¹ż³Ģ)
________________________________________________________________________ӣ
¢Ś¼ĘĖćѳʷ֊n(Cu2£«)(Š“³ö¼ĘĖć¹ż³Ģ)
________________________________________________________________________ӣ
¢Ūøł¾Ż________ŌĄķæÉĒó³ön(K£«)£¬ŌŁŅĄ¾Ż________ŌĄķĒóµĆn(H2O)”£
¢ÜøĆѳʷ¾§ĢåµÄ»ÆѧŹ½ĪŖ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
¹żŃõ»ÆøĘæÉŅŌÓĆÓŚøÄÉʵŲ±ķĖ®ÖŹ£¬“¦Ąķŗ¬ÖŲ½šŹōĮ£×Ó·ĻĖ®ŗĶÖĪĄķ³ą³±£¬Ņ²æÉÓĆÓŚÓ¦¼±¹©ŃõµČ”£¹¤ŅµÉĻÉś²ś¹żŃõ»ÆøʵÄÖ÷ŅŖĮ÷³ĢČēĻĀ£ŗ
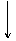
 CaCl2¹ĢĢå””30%µÄH2O2
CaCl2¹ĢĢå””30%µÄH2O2
””””””””””











”””””” ””””””””””””””””””””””””””””
”””””” NH3 ø±²śĘ·”””””” ”””””””””” ””²śĘ·
ŅŃÖŖCaO2·8H2O³Ź°×É«£¬Ī¢ČÜÓŚĖ®£¬¼ÓČČÖĮ350 ”ę×óÓŅæŖŹ¼·Ö½ā·Å³öŃõĘų”£
(1)ÓĆÉĻŹö·½·ØÖĘČ”CaO2·8H2OµÄ»Æѧ·½³ĢŹ½ŹĒ________________________________________________________________________
________________________________________________________________________ӣ
(2)¼ģŃé”°Ė®Ļ“”±ŹĒ·ńŗĻøńµÄ·½·ØŹĒ________”£
(3)³ĮµķŹ±³£ÓƱłĖ®æŲÖĘĪĀ¶ČŌŚ0 ”ę×óÓŅ£¬ĘäæÉÄÜŌŅņŹĒ(Š“³öĮ½ÖÖ)£ŗ
¢Ł________________________________________________________________________£»
¢Ś________________________________________________________________________”£
(4)²ā¶Ø²śĘ·ÖŠCaO2ŗ¬ĮæµÄŹµŃé²½Öč£ŗ
µŚŅ»²½£ŗ×¼Č·³ĘČ”a g²śĘ·ÓŚÓŠČū׶ŠĪĘæÖŠ£¬¼ÓČėŹŹĮæÕōĮóĖ®ŗĶ¹żĮæµÄb g KI¾§Ģ壬ŌŁµĪČėÉŁĮæ2 mol·L£1µÄH2SO4ČÜŅŗ£¬³ä·Ö·“Ó¦”£
µŚ¶ž²½£ŗĻņÉĻŹö׶ŠĪĘæÖŠ¼ÓČė¼øµĪµķ·ŪČÜŅŗ”£
µŚČż²½£ŗÖšµĪ¼ÓČėÅضČĪŖc mol·L£1µÄNa2S2O3ČÜŅŗÖĮ·“Ó¦ĶźČ«£¬ĻūŗÄNa2S2O3ČÜŅŗV mL”£
(ŅŃÖŖ£ŗI2£«2S2O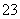 ===2I££«S4O
===2I££«S4O )
)
¢ŁCaO2µÄÖŹĮæ·ÖŹżĪŖ____________(ÓĆ×ÖÄø±ķŹ¾)£»
¢ŚÄ³Ķ¬Ń§µŚŅ»²½ŗĶµŚ¶ž²½µÄ²Ł×÷¶¼ŗÜ¹ę·¶£¬µŚČż²½µĪĖŁĢ«Āż£¬ÕāŃł²āµĆµÄCaO2µÄÖŹĮæ·ÖŹżæÉÄÜ________(Ģī”°²»ŹÜÓ°Ļģ”±”¢”°Ę«µĶ”±»ņ”°Ę«øß”±)£¬ŌŅņŹĒ________________________________________________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ģ¼”¢ĮņµÄŗ¬ĮæÓ°ĻģøÖĢśŠŌÄÜ£¬Ģ¼”¢Įņŗ¬ĮæµÄŅ»ÖÖ²ā¶Ø·½·ØŹĒ½«øÖŃłÖŠĢ¼”¢Įņ×Ŗ»ÆĪŖĘųĢ壬ŌŁÓĆ²āĢ¼”¢²āĮņ×°ÖĆ½ųŠŠ²ā¶Ø”£
(1)²ÉÓĆ×°ÖĆA£¬ŌŚøßĪĀĻĀ½«xæĖøÖŃłÖŠĢ¼”¢Įņ×Ŗ»ÆĪŖCO2”¢SO2”£
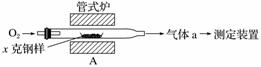
¢ŁĘųĢåaµÄ³É·ÖŹĒ________________”£
¢ŚČōøÖŃłÖŠĮņŅŌFeSŠĪŹ½“ęŌŚ£¬AÖŠ·“Ó¦£ŗ3FeS£«5O2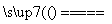
1________£«3________”£
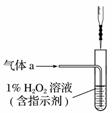
(2)½«ĘųĢåaĶØČė²āĮņ×°ÖĆÖŠ(ČēÓŅĶ¼)£¬²ÉÓƵĪ¶Ø·Ø²ā¶ØĮņµÄŗ¬Į攣
¢ŁH2O2Ńõ»ÆSO2µÄ»Æѧ·½³ĢŹ½
________________________________________________________________________
________________________________________________________________________ӣ
¢ŚÓĆNaOHČÜŅŗµĪ¶ØÉś³ÉµÄH2SO4£¬ĻūŗÄz mL NaOHČÜŅŗ£¬ČōĻūŗÄ1 mL NaOHČÜŅŗĻąµ±ÓŚĮņµÄÖŹĮæĪŖyæĖ£¬ŌņøĆøÖŃłÖŠĮņµÄÖŹĮæ·ÖŹż£ŗ________”£
(3)½«ĘųĢåaĶØČė²āĢ¼×°ÖĆÖŠ(ČēĻĀĶ¼)£¬²ÉÓĆÖŲĮæ·Ø²ā¶ØĢ¼µÄŗ¬Į攣
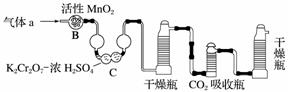
¢ŁĘųĢåaĶعżBŗĶCµÄÄæµÄŹĒ__________________________________________”£
¢Ś¼ĘĖćøÖŃłÖŠĢ¼µÄÖŹĮæ·ÖŹż£¬Ó¦²āĮæµÄŹż¾ŻŹĒ________________________________
________________________________________________________________________ӣ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚ0 ”ę”¢1.01”Į105 PaŹ±½ųŠŠĻĀĮŠŹµŃé£ŗ¼×”¢ŅŅ”¢±ūČżĪ»Ķ¬Ń§ø÷Č”30.0 mLĶ¬ÅØ¶ČµÄŃĪĖį£¬¼ÓČėĻąĶ¬×é³ÉµÄĆ¾ĀĮŗĻ½š·ŪÄ©£¬²ā¶Ø²śÉśĘųĢåµÄĢå»ż£¬ÓŠ¹ŲŹż¾ŻĮŠ±ķČēĻĀ£ŗ
| ŹµŃéŠņŗÅ | ¼× | ŅŅ | ±ū |
| ŗĻ½šÖŹĮæ(mg) | 510 | 765 | 918 |
| ĘųĢåĢå»ż(mL) | 560 | 672 | 672 |
ŹŌĒó£ŗ(1)ŃĪĖįµÄĪļÖŹµÄĮæÅØ¶ČŹĒ¶ąÉŁ£æ
(2)ŗĻ½šÖŠø÷³É·ÖµÄÖŹĮæ·ÖŹż”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓƶčŠŌµē¼«µē½āŅ»¶ØÅØ¶ČµÄCuSO4ČÜŅŗ£¬ĶصēŅ»¶ĪŹ±¼äŗó£¬ĻņĖłµĆµÄČÜŅŗÖŠ¼ÓČė
0£®1 mol Cu(OH)2ŗóĒ”ŗĆ»Öø“µ½µē½āĒ°µÄÅضČŗĶpH”£ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ(””””)
A£®µē½ā¹ż³ĢÖŠŅõ¼«Ć»ÓŠĘųĢåÉś³É
B£®µē½ā¹ż³ĢÖŠ×ŖŅʵĵē×ÓµÄĪļÖŹµÄĮæĪŖ0.4 mol
C£®ŌCuSO4ČÜŅŗµÄÅضČĪŖ0.1 mol·L£1
D£®µē½ā¹ż³ĢÖŠŃō¼«ŹÕ¼Æµ½µÄĘųĢåĢå»żĪŖ2.24 L(±źæöĻĀ)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓĆNaOHČÜŅŗĪüŹÕŃĢĘųÖŠµÄSO2£¬½«ĖłµĆµÄNa2SO3ČÜŅŗ½ųŠŠµē½ā£¬æÉŃ»·ŌŁÉśNaOH£¬Ķ¬Ź±µĆµ½H2SO4£¬ĘäŌĄķČēĻĀĶ¼ĖłŹ¾(µē¼«²ÄĮĻĪŖŹÆÄ«)”£
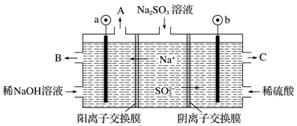
(1)Ķ¼ÖŠa¼«ŅŖĮ¬½ÓµēŌ“µÄ________(Ģī”°Õż”±»ņ”°øŗ”±)¼«£¬CæŚĮ÷³öµÄĪļÖŹŹĒ________”£
(2)SO ·ÅµēµÄµē¼«·“Ó¦Ź½ĪŖ____________”£
·ÅµēµÄµē¼«·“Ó¦Ź½ĪŖ____________”£
(3)µē½ā¹ż³ĢÖŠŅõ¼«Ēų¼īŠŌĆ÷ĻŌŌöĒ棬ÓĆĘ½ŗāŅʶÆŌĄķ½āŹĶŌŅņ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
PbO2æÉÓÉPbOÓė“ĪĀČĖįÄĘČÜŅŗ·“Ó¦ÖĘµĆ£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ________________________________£»PbO2Ņ²æÉŅŌĶعżŹÆÄ«ĪŖµē¼«£¬Pb(NO3)2ŗĶCu(NO3)2µÄ»ģŗĻČÜŅŗĪŖµē½āŅŗµē½āÖĘČ””£Ńō¼«·¢ÉśµÄµē¼«·“Ó¦Ź½ĪŖ__________________________£¬Ņõ¼«ÉĻ¹Ū²ģµ½µÄĻÖĻóŹĒ________________£»Čōµē½āŅŗÖŠ²»¼ÓČėCu(NO3)2£¬Ņõ¼«·¢ÉśµÄµē¼«·“Ó¦Ź½ĪŖ________________________£¬ÕāŃł×öµÄÖ÷ŅŖȱµćŹĒ________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Į½øöÓŠĮŖĻµµÄ²»Ķ¬·“Ó¦Ļą±Č
C(s)£«O2(g)===CO2(g)””¦¤H1<0
C(s)£« O2(g)===CO(g)””¦¤H2<0
O2(g)===CO(g)””¦¤H2<0
Ōņ¦¤H1____¦¤H2”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com