
| A. | ①③⑥⑧ | B. | ③④⑤⑥ | C. | ②④⑤⑦⑧ | D. | ②④⑤⑦ |
分析 ①非金属性越强,对应最高价含氧酸的酸性越强;
②碳酸氢钠加热分解生成碳酸钠;
③同主族从上到下非金属性减弱;
④水分子间含氢键;
⑤NaOH在水中完全电离,而一水合氨部分电离;
⑥非金属性越强,对应氢化物越稳定;
⑦HI不如HCl稳定,则在水中H-I易断裂;
⑧非金属性越强,对应氢化物还原性越弱.
解答 解:①非金属性越强,对应最高价含氧酸的酸性越强,则酸性:H2SO4>H3PO4,能用元素周期律解释,故不选;
②碳酸氢钠加热分解生成碳酸钠,可知热稳定性:Na2CO3>NaHCO3,不能用元素周期律解释,故选;
③同主族从上到下非金属性减弱,则非金属性:Cl>Br,能用元素周期律解释,故不选;
④水分子间含氢键,可知熔点:H2O>H2S,不能用元素周期律解释,故选;
⑤NaOH在水中完全电离,而一水合氨部分电离,则碱性:NaOH>NH3•H2O,不能用元素周期律解释,故选;
⑥非金属性越强,对应氢化物越稳定,则稳定性:H2O>H2S,能用元素周期律解释,故不选;
⑦HI不如HCl稳定,则在水中H-I易断裂,则酸性:HI>HCl,不能用元素周期律解释,故选;
⑧非金属性越强,对应氢化物还原性越弱,则还原性:HI>HCl,能用元素周期律解释,故不选;
故选D.
点评 本题考查周期表及元素周期律的综合应用,为高频考点,把握元素的位置、性质及元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
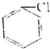 ②
② ③(CH3)3CCH2Cl ④CHCl-CHBr2⑤
③(CH3)3CCH2Cl ④CHCl-CHBr2⑤ ⑥CH3Cl.
⑥CH3Cl.| A. | ②③⑤ | B. | ①③⑥ | C. | 全部 | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑥⑦ | B. | ②③⑤⑧⑨ | C. | ②③⑥⑦⑨ | D. | ①④⑤⑧⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
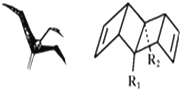 始祖鸟烯形状宛如一只展翅低头飞翔的鸟,其键线式结构表示如图,其中R 1、R 2为烷烃基.则下列有关始祖鸟烯的说法中正确的是( )
始祖鸟烯形状宛如一只展翅低头飞翔的鸟,其键线式结构表示如图,其中R 1、R 2为烷烃基.则下列有关始祖鸟烯的说法中正确的是( )| A. | 始祖鸟烯与乙烯互为同系物 | |
| B. | 若R 1=R 2=甲基,则其化学式为C 12H 16 | |
| C. | 若R 1=R 2=甲基,则始祖鸟烯的一氯代物有3种 | |
| D. | 始祖鸟烯既能使酸性高锰酸钾溶液褪色,也能使溴水褪色,则两反应的反应类型是相同的 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
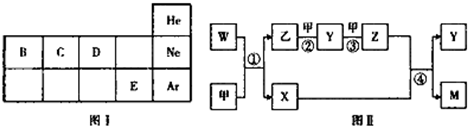
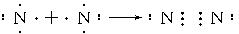 ,Y的分子式为NO,W的结构式为
,Y的分子式为NO,W的结构式为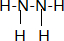 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯的分子式为C6H6,它不能使酸性KMnO4溶液褪色,属于饱和烃 | |
| B. | 从苯的结构简式 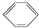 看,苯分子中含有碳碳双键,应属于烯烃 看,苯分子中含有碳碳双键,应属于烯烃 | |
| C. | 在催化剂作用下,苯与液溴反应生成溴苯,发生了加成反应 | |
| D. | 苯分子为平面正六边形结构,6个碳原子之间的化学键完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
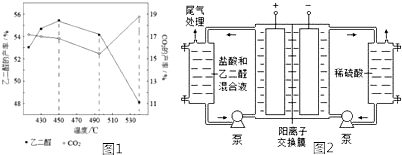
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com