
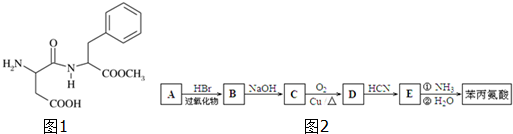
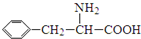 )是合成APM的原料之一.苯丙氨酸的一种合成途径如图2所示:
)是合成APM的原料之一.苯丙氨酸的一种合成途径如图2所示: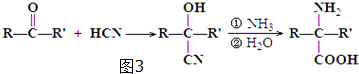
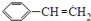 .
.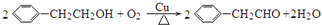 .
. .
. 分析 (1)根据APM的结构简式,可知其分子式,APM中有羧基、酯基、肽键、氨基等官能团,据此判断;
(2)APM在人体胃肠道酶作用下,酯基和肽键都能发生水解,在生成的产物中,相对分子质量最小的是CH3OH,据此答题;
(3)由苯丙氨酸(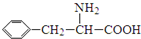 )的结构简式结合信息(2)可知,E为
)的结构简式结合信息(2)可知,E为 ,D为
,D为 ,根据各物质转化关系可进一步推断得C为
,根据各物质转化关系可进一步推断得C为 ,B为
,B为 ,A为
,A为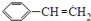 ,A发生加成生成B,B发生水解生成C,C氧化得D,D发生加成得E,据此答题.
,A发生加成生成B,B发生水解生成C,C氧化得D,D发生加成得E,据此答题.
解答 解:(1)A.APM中有氮元素,不属于糖类化合物,故A错误;
B.根据APM的结构简式,可知其分子式为C14H18N2O5,故B正确;
C.APM中有氨基能与酸反应,有羧基能与碱反应,故C正确;
D.APM中有羧基能发生酯化反应,有苯环,能与氢气等发生加成反应,故D错误;
故选:BC;
(2)APM在人体胃肠道酶作用下,酯基和肽键都能发生水解,在生成的产物中,相对分子质量最小的是CH3OH,其官能团名称为羟基,
故答案为:CH3OH;羟基;
(3)由苯丙氨酸(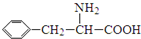 )的结构简式结合信息(2)可知,E为
)的结构简式结合信息(2)可知,E为 ,D为
,D为 ,根据各物质转化关系可进一步推断得C为
,根据各物质转化关系可进一步推断得C为 ,B为
,B为 ,A为
,A为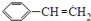 ,A发生加成生成B,B发生水解生成C,C氧化得D,D发生加成得E,
,A发生加成生成B,B发生水解生成C,C氧化得D,D发生加成得E,
①根据上面的分析可知,D→E的反应类型为加成反应,故答案为:加成反应;
②根据上面的分析可知,A的结构简式为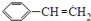 ,故答案为:
,故答案为: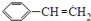 ;
;
③C→D反应的化学方程式为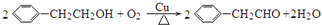 ,故答案为:
,故答案为: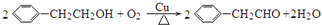 ;
;
④某苯的同系物苯环上的一硝基取代物只有一种,该硝基取代物W是苯丙氨酸的同分异构体,W的结构简式为 ,故答案为:
,故答案为: .
.
点评 本题考查有机物的合成,题目难度中等,解答本题的关键是能全面、准确把握题给信息,答题时注意审题,加强自学能力的培养.


科目:高中化学 来源: 题型:选择题
| A. | 1.7克氢氧根离子(OH-)含有的电子数为 NA | |
| B. | 7克乙烯(CH2=CH2)所含的电子数为4NA | |
| C. | 标准状况下,22.4L一氧化碳所含的分子数为 NA | |
| D. | 1molFe分别与氯气和硫反应失去电子都是3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反应装置如图.下列对该实验的描述错误的是( )
1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反应装置如图.下列对该实验的描述错误的是( )| A. | 控制温度不可以用水浴加热 | |
| B. | 长玻璃管起冷凝回流作用 | |
| C. | 提纯乙酸丁酯需要经过氢氧化钠溶液洗涤 | |
| D. | 加入过量乙酸可以提高1-丁醇的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.7 g羟基(-OH)中含有的电子数为NA | |
| B. | 标准状况下,11.2 L CCl4含有的碳原子数为0.5NA | |
| C. | 1 mol苯分子中含有的碳碳双键数为3NA | |
| D. | 常温下,28g乙烯中含有的碳原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=1的溶液中:Fe2+、CH3COO-、K+、SO42- | |
| B. | 在含较多Al3+的溶液中:Na+、Cl-、HCO3- | |
| C. | 在0.1 mol•L-1 CaCl2溶液中:K+、Ba2+、I-、OH- | |
| D. | 在$\frac{c({H}^{+})}{c(O{H}^{-})}$=10-12的溶液中:K+、Na+、ClO-、NO${\;}_{3}^{-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 叙述I | 叙述II |
| A | Fe3+的氧化性比Cu2+强 | FeCl3溶液可用于溶解回收旧电路板中的铜 |
| B | NH4Cl受热分解 | 加热可将Ca(OH)2和NH4Cl固体混合物分离 |
| C | 金属活动性铜比铁弱 | 镀铜铁制品表层划损后仍然受到保护 |
| D | Cl2具有漂白性 | 用氯气制盐酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴定 次数 | 待测溶液的 体积/mL | 标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 跟水反应时,水作氧化剂 | |
| B. | NaH中H-半径比Li+半径小 | |
| C. | NaH跟液氨反应时,有NaNH2生成 | |
| D. | Na原子与H原子结合组成NaH过程中发生了电子转移. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com