
碳酸镁晶须是一种新型的吸波隐形材料中的增强材料。
(1)合成该物质的步骤如下:
步骤1:配制0.5 mol·L-1 MgSO4溶液和0.5 mol·L-1 NH4HCO3溶液。
步骤2:用量筒量取500 mL NH4HCO3溶液于1 000 mL四口烧瓶中,开启搅拌器,温度控制在50 ℃。
步骤3:将250 mL MgSO4溶液逐滴加入NH4HCO3溶液中,1 min内滴加完后,用氨水调节溶液pH到9.5。
步骤4:放置1 h后,过滤,洗涤。
步骤5:在40 ℃的真空干燥箱中干燥10 h,得碳酸镁晶须产品(MgCO3·nH2O n=1~5)。
回答下列问题:
①步骤3中加氨水后的离子方程式_______________________________________。
②步骤4为加快过滤速度,常用________________________________________(填过滤方法)。

(2)测定合成的MgCO3·nH2O中的n值。
称量1.000 g碳酸镁晶须,放入右图所示的广口瓶中,加入适量水,滴入稀硫酸与晶须反应,生成的CO2被NaOH溶液吸收,在室温下反应4~5 h,反应后期将温度升到30 ℃,最后的烧杯中的溶液用已知浓度的盐酸滴定,测得CO2的总量;重复上述操作2次。
①图中气球的作用是________________________________________________________;
②上述反应后期要升温到30 ℃,主要目的是_______________________________________;
③设3次实验测得每1.000 g碳酸镁晶须产生的CO2平均值为a mol,则n值为________________________(用含a的表达式表示)。
(3)称取100 g上述晶须产品进行热重分析,热重曲线如下图。则该条件下合成的晶须中,n=____________(选填:1、2、3、4、5)。

答案 (1)①Mg2++NH3·H2O+HCO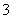 ===MgCO3↓+NH
===MgCO3↓+NH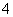 +H2O ②减压过滤(或抽滤)
+H2O ②减压过滤(或抽滤)
(2)①暂时储存CO2,有利于CO2被NaOH溶液吸收,且能保持装置中压强相对稳定 ②升高温度气体的溶解度减小,使溶解在水中的CO2逸出,便于吸收完全
③(1-84a)/18a
(3)1
解析 (1)①加入氨水促进HCO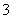 的电离,适当增大CO
的电离,适当增大CO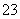 的浓度。②加快过滤的方法只能是减压过滤。
的浓度。②加快过滤的方法只能是减压过滤。
(2)①开始产生的CO2速率大于NaOH溶液吸收CO2的速率,气球逐渐胀大,暂时储存CO2,避免产生的CO2使内部压强过大,造成气体泄漏;后期CO2被NaOH吸收时,气球逐渐变小;②使溶解在水中的CO2逸出,便于吸收完全;
③找出关系:MgCO3·nH2O~CO2
84+18n 1
1.000 a
得n=(1.000-84a)/18a
(3)从图中看,剩余质量为82.3 g时,减少的质量为失去的结晶水的质量;剩余39.5 g时,减少的质量为分解出的CO2的质量,列式:100 g×18n/(84+18n)=100 g-82.3 g,得n=1。


科目:高中化学 来源: 题型:
下列事实不能用有机物分子内基团间的相互作用解释的是( )
A.乙烯能发生加成反应而乙烷不能
B.苯酚能跟NaOH溶液反应而乙醇不能
C. 甲苯能使KMnO4酸性溶液褪色而乙烷不能
D.苯在50℃~60℃时发生硝化反应而甲苯在30℃时即可
查看答案和解析>>
科目:高中化学 来源: 题型:
反应4NH3+5O2 ===== 4NO+6H2O在5L的密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则此反应的平均速率表达正确的是
A. v(O2)=0.01mol/(L•S) B. v(NO)=0.008mol/(L•S)
C. v(H2O)=0.003mol/(L•S) D. v(NH3)=0.004mol/(L•S)
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中,将1.0mol CO与1.0mol H2O混合加热到800℃,发生下列反应:CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
一段时间后该反应达到平衡,测得CO的物质的量为0.5mol。回答下列问题:
①平衡时CO的转化率为 ,该反应的化学平衡常数为 。
②如果继续向该平衡体系中通入1.0mol的H2O(g),相同条件下反应达到新的平衡状态,则CO的转化率将 (填“增大”、“减小”、“不变”),预计CO的转化率为 。
③427℃时该反应的平衡常数为9.4,请结合①中的计算结果判断该反应的△H 0(填“>”、“==”、“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
碘在科研与生活中有重要应用。某兴趣小组用0.50 mol·L-1 KI、0.2%淀粉溶液、0.20 mol·L-1 K2S2O8、0.10 mol·L-1 Na2S2O3等试剂,探究反应条件对化学反应速率的影响。
已知:S2O +2I-===2SO
+2I-===2SO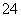 +I2 (慢)
+I2 (慢)
I2+2S2O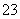 ===2I-+S4O
===2I-+S4O (快)
(快)
(1)向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中的________________耗尽后,溶液颜色将由无色变为蓝色。为确保能观察到蓝色,S2O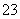 与S2O
与S2O 初始的物质的量需满足的关系为n(S2O
初始的物质的量需满足的关系为n(S2O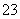 )∶n(S2O
)∶n(S2O )________________。
)________________。
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
| 实验序号 | 体积V/mL | ||||
| K2S2O8溶液 | 水 | KI溶液 | Na2S2O3溶液 | 淀粉溶液 | |
| ① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
| ② | 9.0 | 1.0 | 4.0 | 4.0 | 2.0 |
| ③ | 8.0 | Vx | 4.0 | 4.0 | 2.0 |
表中Vx=______________,理由是___________________________。
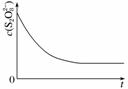
(3)已知某条件下,浓度c(S2O )~反应时间t的变化曲线如图所示,若保持其他条件不变,请在坐标图中,分别画出降低反应温度和加入催化剂时c(S2O
)~反应时间t的变化曲线如图所示,若保持其他条件不变,请在坐标图中,分别画出降低反应温度和加入催化剂时c(S2O )~t的变化曲线示意图(进行相应的标注)。
)~t的变化曲线示意图(进行相应的标注)。
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下表信息,判断以下叙述正确的是 ( )
部分短周期元素的原子半径及主要化合价
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.102 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
A.R与T形成的化合物RT3中,各原子均满足8电子的稳定结构
B.单质与稀盐酸反应产生氢气的剧烈程度为L<Q
C.M与T形成的化合物具有两性
D.L2+与R2-的核外电子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
人们把NaHCO3作为发酵粉使用时,往往加入少量的明矾,这样做的目的是( )
A.明矾能起催化剂作用
B.碳酸氢钾比碳酸氢钠更易分解
C.明矾受热分解放出气体
D.铝盐在水中能起到酸的作用
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示,这四种元素的原子最外层电子数之和为20。则下列说法不正确的是
 A.最高价氧化物的水化物的酸性:X<Z
A.最高价氧化物的水化物的酸性:X<Z
B.原子半径大小:Y<X<W
C.氢化物的稳定性X<Y
D.X和Y形成的化合物升华破坏的是共价键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com