
下面是实验室制取少量固体氧化铜的实验,根据实验步骤,回答有关问题。
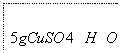 —→
—→ —→
—→
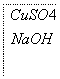 —→
—→ —→
—→
 —→
—→ —→
—→
(1)调整天平零点时,若指针偏向左边,应将左边的螺丝________(填“向左”或“向右”)旋动。
(2)溶解样品时要用到玻璃棒,其作用是_ ________________________________ ___________________________________________________________________。
(3)反应生成沉淀的离子方程式为______________________________________ ______________________________________________________________。
(4)加热蒸发过程中要用到玻璃棒,其作用是_ __________________________________ _________________________________________________________________。
(5)过滤中要用到玻璃棒,其作用是_________________________ _________________________。
(6)洗涤沉淀的目的是
__________________________________________________;
洗涤沉淀的方法是
__________________________________________________;
为了检验沉淀是否洗涤干净,应在最后一次的洗涤液中加入________溶液。
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
已知某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用如图所示的装置进行实验。
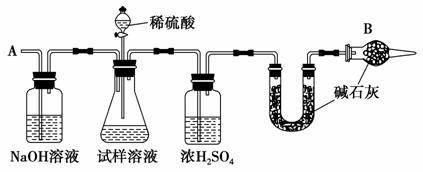
主要实验步骤如下:
①按照图示组装仪器,并检查装置的气密性
②将a g试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液
③称量盛有碱石灰的U形管的质量为b g
④从分液漏斗滴入6 mol·L-1的稀硫酸,直到不再产生气体为止
⑤从导管A处缓缓鼓入一定量的空气
⑥再次称量盛有碱石灰的U形管的质量为c g
⑦重复步骤⑤和⑥的操作,直到U形管的质量基本不变,为d g
请回答下列问题:
(1)在用托盘天平称量样品时,如果天平的指针向左偏转,说明________________________________________________________________________。
(2)装置中干燥管B的作用是_____________________________________。
(3)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测量的结果将________(填“偏高”、“偏低”或“不变”)。
(4)步骤⑤的目的是________________________________________。
(5)步骤⑦的目的是_______________________________________________。
(6)试样中纯碱的质量分数为________________(用含a、b、d的代数式表示)。
(7)还可以用其他实验方法测定试样中纯碱的质量分数,请简述一种不同的实验方法_______________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
图1和图2分别是1s电子的概率分布图和原子轨道图。下列有关认识正确的是
( )。

A.图1中的每个小黑点表示1个电子
B.图2表示1s电子只能在球体内出现
C.图2表明1s轨道呈圆形,有无数对称轴
D.图1中的小黑点表示某一时刻,电子在核外所处的位置
查看答案和解析>>
科目:高中化学 来源: 题型:
下述实验设计能够达到目的的是 ( )。
| 选项 | 实验目的 | 实验设计 |
| A | 除去CO2中少量的SO2 | 将混合气体通过饱和Na2CO3溶液 |
| B | 除去Cu粉中混有的CuO | 向混合物中滴加适量稀硝酸 |
| C | 检验溶液中是否含有Fe2+ | 向溶液中滴入氯水后,再滴加KSCN溶液 |
| D | 证明H2CO3酸性比H2SiO3强 | 将CO2通入Na2SiO3溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列实验事实得出的结论正确的是 ( )。
A.气体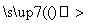 品红溶液褪色
品红溶液褪色
结论:原气体一定是SO2
B.气体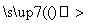 气体
气体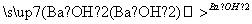 白色沉淀
白色沉淀
结论:原气体一定是烃
C.某溶液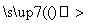 冒白雾
冒白雾 白烟
白烟
结论:原溶液一定是浓盐酸
D.某有色溶液 紫色
紫色
结论:原溶液中一定含有Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
对下列各组物质关系的描述中不正确的是( )
A.O2和O3互为同素异形体
B.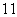 H、
H、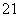 H和
H和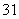 H互为同位素
H互为同位素
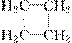 |
C.CH2===CH2和 互为同系物
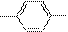 | |||
 | |||
D. C2H5和H3C CH3互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)分子式为C4H10O并能与金属钠反应放出H2的有机化合物有________种。
(2)与化合物C7H10O2互为同分异构体的物质不可能为________。
A.醇 B.醛
C.羧酸 D.酚
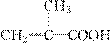 |
(3)与 具有相同官能团的同分异构体的结构简式为
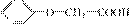 _______________。
_______________。
(4)苯氧乙酸( )有多种酯类的同分异构体。其中能与FeCl3溶
液发生显色反应,且苯环上有2种一硝基取代物的同分异构体是_________________(写出任意2种的结构简式)。
(5)分子式为C5H10的烯烃共有(不考虑顺反异构)________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,将这些气体与1.68 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5 mol·L-1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
A.60 mL B.45 mL
C.30 mL D.15 mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com