
 利用Fe+CuSO4=Cu+FeSO4设计一个原电池.画出实验装置图. 并指出:
利用Fe+CuSO4=Cu+FeSO4设计一个原电池.画出实验装置图. 并指出:分析 根据原电池工作原理结合总反应方程式,还原剂作负极,不如负极活泼的金属或非金属导体作正极,氧化剂的溶液作电解质溶液,由此分析解答.
解答 解:不如负极活泼的金属或导电的分金属作正极,根据反应方程式,可选铜作正极,正极上铜离子得电子生成铜单质,电极反应式为:Cu2++2e-═Cu,而CuSO4+Fe═FeSO4+Cu,该反应中,铁失电子生成二价铁离子进入溶液,所以铁作还原剂,电极反应式为:Fe-2e-═Fe2+;实验装置图为: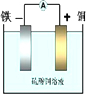 ,
,
故答案为:Cu(或C等),Cu2++2e-=Cu;Fe; Fe-2e-=Fe2+.
点评 本题考查了原电池的设计,原电池的设计关键是负极材料和电解质溶液的成分,一般来说,还原剂作负极,不如负极活泼的金属或非金属导体作正极,氧化剂的溶液作电解质溶液.


 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源: 题型:选择题
| A. | 离子化合物中一定不含共价键 | |
| B. | 共价化合物中一定不含离子键 | |
| C. | 两种元素组成的化合物中一定不含非极性键 | |
| D. | 氢键只存在于分子之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同分异构体 | B. | 不同密度的核素 | C. | 同位素 | D. | 同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3种 | B. | 6种 | C. | 9 种 | D. | 12种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④①③② | B. | ①④③② | C. | ①②③④ | D. | ④③①② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 的性质叙述不正确的是( )
的性质叙述不正确的是( )| A. | 能使溴水褪色 | |
| B. | 能使酸性高锰酸钾溶液褪色 | |
| C. | 能发生加成反应 | |
| D. | 能发生加聚反应,且生成的聚合物也能使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大反应物的量,化学反应速率一定加快 | |
| B. | 气体反应体系的压强增大,化学反应速率一定加快 | |
| C. | 与金属锌反应时,硫酸的浓度越大,产生H2速率越快 | |
| D. | 2molX气体在2L的容器中反应,4s后浓度变为0.5mol•L-1,则其反应速率为0.125mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com