
| 1.NaOH溶液 |
| 2.稀硫酸 |
| 1.NaOH溶液 |
| 2.稀硫酸 |
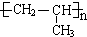 ;C的氢谱图有3个峰,面积比为3:2:1,应含有3个酚羟基,C的结构简式为
;C的氢谱图有3个峰,面积比为3:2:1,应含有3个酚羟基,C的结构简式为 ,则A为
,则A为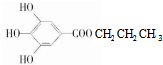 ,据此解答.
,据此解答.| 1.NaOH溶液 |
| 2.稀硫酸 |
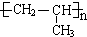 ;C的氢谱图有3个峰,面积比为3:2:1,应含有3个酚羟基,C的结构简式为
;C的氢谱图有3个峰,面积比为3:2:1,应含有3个酚羟基,C的结构简式为 ,则A为
,则A为 ,
,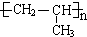 ,
, ;
;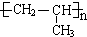 ;
; +H2O
+H2O| (1)NaOH溶液 |
| (2)浓硫酸 |
 +CH3CH2CH2OH;
+CH3CH2CH2OH;| 浓硫酸 |
| 170℃ |
 +H2O
+H2O| (1)NaOH溶液 |
| (2)浓硫酸 |
 +CH3CH2CH2OH;
+CH3CH2CH2OH;| 浓硫酸 |
| 170℃ |
 有多种同分异构体,满足下列条件:①含苯环 ②能发生银镜反应 ③不能发生水解反应,符合条件的2种同分异构体的结构简式为:
有多种同分异构体,满足下列条件:①含苯环 ②能发生银镜反应 ③不能发生水解反应,符合条件的2种同分异构体的结构简式为: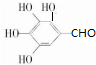 、
、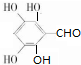 等,
等, 、
、 ;
; ,官能团为酚羟基、羧基,故答案为:酚羟基、羧基;
,官能团为酚羟基、羧基,故答案为:酚羟基、羧基;

科目:高中化学 来源: 题型:
| 实验 试剂/mL | 甲 | 乙 | 丙 | 丁 |
| 4mol/L H2SO4 | 20 | V1 | V2 | V3 |
| 饱和CuSO4溶液 | 0 | 2.5 | V4 | 10 |
| H2O | V5 | V6 | 8 | 0 |
| A、实验甲产生气泡的速率最快 |
| B、V1<V2<V3<20 |
| C、V4=V5=10 |
| D、V6=7.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:


| 密度 (g/cm3) | 熔点 (℃) | 沸点 (℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
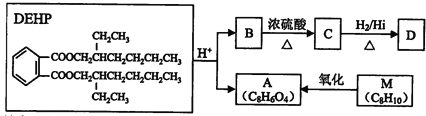
查看答案和解析>>
科目:高中化学 来源: 题型:
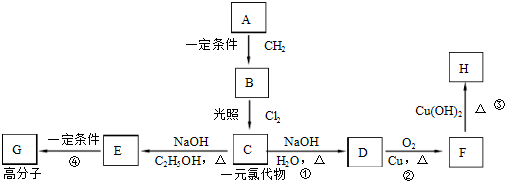
查看答案和解析>>
科目:高中化学 来源: 题型:
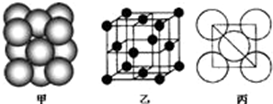 ①若某金属M为第四周期单电子数最多的元素,该元素在周期表中的位置
①若某金属M为第四周期单电子数最多的元素,该元素在周期表中的位置查看答案和解析>>
科目:高中化学 来源: 题型:
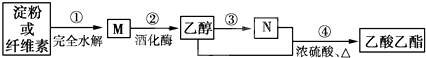
| A、M的分子式为C6H12O6 |
| B、用NaOH溶液可除去乙酸乙酯中混有的乙酸 |
| C、①、④的反应类型均属于取代反应 |
| D、N的化学式为CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
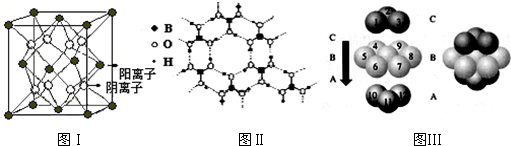
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com