
| A、产物B的状态可能为固态或液态 |
| B、平衡时,单位时间内A和B消耗的物质的量之比为1:1 |
| C、保持体积不变,向平衡体系中加入A(s),平衡不移动 |
| D、若开始时向容器中加入1molB和1molC,达到平衡时放出热量QkJ |


科目:高中化学 来源: 题型:
| A、离子半径:F->Na+>Mg2+>Al3+ |
| B、热稳定性:HCl>H2S>PH3>AsH3 |
| C、酸性强弱:H3AlO3<H4SiO4<H2CO3<H3PO4 |
| D、沸点:HF<HCl<HBr<HI |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、雾霾的主要组成是二氧化硫、氮氧化物和可吸入颗粒物 |
| B、垃圾是放错地方的资源,应分类回收利用 |
| C、光导纤维是一种无机非金属材料,现已广泛应用于太阳能电池的生产 |
| D、14C可用于文物的年代鉴定,14C和12C互为同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、F2、Cl2、Br2、I2的熔、沸点逐渐升高 |
| B、NH3易液化 |
| C、HF、HCl、HBr、HI的热稳定性依次减弱 |
| D、H2S的熔沸点低于H2O的熔、沸点 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、热稳定性:HF>HCl>HBr |
| B、原子半径:Na>S>O |
| C、离子半径:Mg2+>O2->F- |
| D、酸性:HClO4>H2SO4>H3PO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
| A、电池放电时,镍元素被氧化 |
| B、电池充电时,氢元素被还原 |
| C、电池放电时,镍元素被还原 |
| D、电池充电时,H2在阴极生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、混有乙酸、乙醇杂质的乙酸乙酯用饱和Na2CO3溶液进行除杂 |
| B、往FeCl2溶液中滴入KSCN溶液,检验FeCl2是否已氧化变质 |
| C、实验证实不存在两种邻-二甲苯,故现代结构理论认为苯分子中碳碳键完全不是单双键交替结构 |
| D、两种有机物质若具有相同的相对分子质量和不同的结构,则一定互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
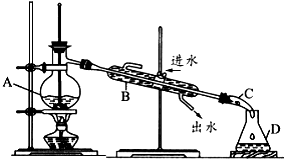
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、混合溶液的pH一定等于7 |
| B、如果混合溶液的pH大于7,则碱一定为弱碱 |
| C、如果碱是强碱,则pH一定大于7 |
| D、如果酸是强酸,则pH一定小于7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com