
【题目】下列变化不能用勒夏特列原理解释的是
A.工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率
B.工业上合成氨要用高温,催化剂
C.红棕色的NO2加压后颜色先变深再变浅
D.CO2(g)![]() CO2(aq)ΔH<0,降温增压可增大二氧化碳气体在水中的溶解度
CO2(aq)ΔH<0,降温增压可增大二氧化碳气体在水中的溶解度
科目:高中化学 来源: 题型:
【题目】有机合成在化工医药领域应用广泛,下图是一种新型药物合成路线。
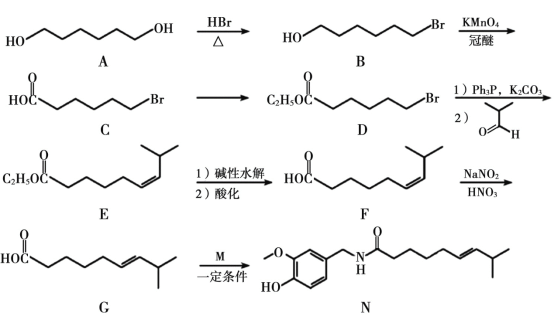
回答下列问题:
(1)A 的系统命名法(CCS)名称为________,D 中官能团的名称为________。
(2)B→C 的反应类型为________,从反应所得液态有机混合物中提纯 B 的常用方法为________。
(3)C→D 的化学方程式为________。C 和 D 在下列哪种检测仪上显示出的信号峰是完全相同的_________
A.元素分析仪 b.红外光谱仪 c.核磁共振仪 d.质谱仪
(4)C 的同分异构体 W(不考虑手性异构)可发生银镜反应,且 1 mol W 最多与 2 molNaOH 发生反应,产物之一可被氧化成二元醛,满足上述条件的 W 有________种。若 W 的核磁共振氢谱具有四组峰,则其结构简式为________。
(5)F 与 G 的关系为(填序号)________。
A.碳链异构 b.官能团类别异构 c.顺反异构 d.官能团位置异构
(6)M 的结构简式为________。
(7)参照上述合成路线,以![]() 和
和![]() 为原料制备医药中间体
为原料制备医药中间体![]() ,写出合成路线流程图_________________________________________________________________。
,写出合成路线流程图_________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CxHy+H2O→CO+CO2+H2(未配平),工业上用甲烷、乙烷的混合气体利用上述反应生成氢气,反应后气体经干燥组成如下表所示,计算原混合气体中甲烷与乙烷的物质的量之比____________。
组分 | CO | CO2 | H2 |
体积分数 | 20% | 5% | 75% |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填写下列空白
(1)写出Na2O2的电子式_____
(2)Al(OH)3在碱性溶液中的电离方程式为_____
(3)用离子方程式表示Na2S溶液呈碱性的原因_____
(4)在锌粒与稀硫酸的反应体系中,若滴加几滴CuSO4溶液,发现放出气体的速率明显加快,说明其原因:_____;若加入少量醋酸钠固体,发现放出气体的速率明显减慢,说明其原因_____。
(5)用惰性电极电解U形管中的饱和食盐水(已滴加酚酞),_____极附近溶液会变红。写出用惰性电极电解氯化铜溶液的化学反应方程式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,将前者加入后者时,无论前者是否过量,都能用同一个化学方程式表示的是( )
A. 盐酸 Na2CO3溶液 B. 氢氧化钠溶液 AlCl3溶液
C. Cl2 铁粉 D. CO2 澄清石灰水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新型纳米材料MFe2Ox(3<x<4)中M表示+2价的金属元素,在反应中化合价不发生变化。常温下,MFe2Ox能使工业废气中的SO2转化为S,流程如下:
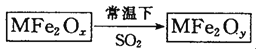
则下列判断正确的是( )
A.x>yB.MFe2Ox是还原剂C.SO2是该反应的催化剂D.SO2发生了置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究小组探究外界条件对化学反应mA(g)+n(B)(g) ![]() pC(g)的速率和平衡的影响图像如下,下列判断正确的是( )
pC(g)的速率和平衡的影响图像如下,下列判断正确的是( )
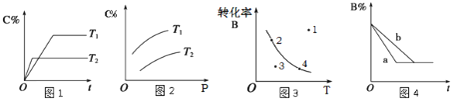
A.由图1可知,T1<T2,该反应正反应为吸热反应
B.由图2可知,该反应m+n<p
C.图3中,表示反应速率v(正)>v(逆)的是点3
D.图4中,若m+n=p,则a曲线一定使用了催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.《抱朴子》中“丹砂烧之成水银,积变又还成丹砂”两个反应互为可逆反应
B.电热水器用镁棒防止内胆腐蚀,原理是牺牲阴极的阳极保护法
C.门捷列夫根据元素的性质随着相对原子质量递增呈现周期性变化规律,制出了第一张元素周期表
D.石灰乳与海水混合,过滤得![]() ,将其溶于盐酸,再蒸发结晶得到
,将其溶于盐酸,再蒸发结晶得到![]() ,电解熔融
,电解熔融![]() 可得到金属镁
可得到金属镁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,NH3·H2O的Kb=1.8×10-5,H2SO3的Ka1=1.3×10-2,Ka2=6.2×10-8。氨水可用于工业尾气中SO2的吸收。下列指定溶液中微粒的物质的量浓度关系正确的是( )
A.氨水与SO2反应恰好生成(NH4)2SO3时:c(NH4+)>c(SO32-)>c(OH-)>c(H+)
B.氨水与SO2反应所得溶液pH=9时:c(NH4+)+c(H+)<3c(HSO3-)+c(OH-)
C.氨水与SO2反应生成等物质的量NH4HSO3和(NH4)2SO3时:3c(NH4+)+3c(NH3·H2O)=2c(SO32-)+2c(HSO3-)+2c(H2SO3)
D.氨水与SO2反应恰好生成NH4HSO3时:c(H+)+c(H2SO3)=c(OH-)+c(SO32-)+c(NH3·H2O)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com