


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
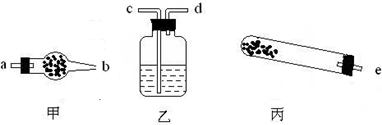
| 仪器 | 试管 | 干燥管 干燥管 |
洗气瓶 洗气瓶 |
| 药品 | 碱式碳酸铜 | 无水硫酸铜 无水硫酸铜 |
澄清石灰水 澄清石灰水 |
| △ |
| △ |
| ||
| ||
| 22400w-65V |
| 64V |
| 22400w-65V |
| 64V |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 (2013?闸北区二模)含有硫的化合物在工业生产中应用广泛,回答下列问题:
(2013?闸北区二模)含有硫的化合物在工业生产中应用广泛,回答下列问题:| 装置 | A (试管+粉末) |
B | C |
| 反应前 | 42.0g | 75.0g | 140.0g |
| 反应后 | 37.0g | 79.0g | 140.5g |
| 高温 |
| 高温 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
现有25℃的硫酸铜饱和溶液300克,加热蒸发掉80克水后,再冷却到原来的温度,求析出CuSO4·5H2O多少克(已知25℃时,CuSO4的溶解度为20克)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com