
高温下,炽热的铁与水蒸气在一个体积可变的密闭容器中进行反应:
3Fe(s)+4H2O(g)=Fe3O4(s)+4H2(g),下列条件的改变对其反应速率几乎无影响的是 ( )
A.把铁块变成铁粉 B.将容器的体积缩小一半
C.压强不变,充入氮气使容器体积增大 D.体积不变,充入氮气使容器压强增大
科目:高中化学 来源: 题型:
下列有关硫元素及其化合物的说法或描述正确的是 ( )
A.硫黄矿制备硫酸经历两步:S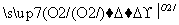 SO3
SO3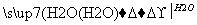 H2SO4
H2SO4
B.酸雨与土壤中的金属氧化物反应后,硫元素以单质的形式进入土壤中
C.在燃煤中加入石灰石可减少SO2排放,发生的反应为2CaCO3+2SO2+O2===2CO2+2CaSO4
D.土壤中的闪锌矿(ZnS)遇到硫酸铜溶液转化为铜蓝(CuS),说明CuS很稳定,不具有还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A.乙二醇和丙三醇互为同系物
B.甲烷、乙烯和苯在工业上都可通过石油分馏得到
C.可通过酸性高锰酸钾溶液来区别烯烃和炔烃
D.苯酚对皮肤有腐蚀性,如果不慎粘到手上,应该立即用酒精清洗
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)若5.2g乙炔(C2H2气态)完全燃烧生成液态水和CO2(g)时放热260kJ。该反应的热化学方程式为 ;
乙炔的燃烧热为 。
(2)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
__________________________________________________________________________。
(3)已知:
2Fe(s)+O2(g)=2FeO(s) ΔH=-544.0kJ·mol-1
4Al(s)+3O2(g)=2Al2O3(s) ΔH=-3351.4kJ·mol-1
则Al和FeO发生铝热反应的热化学方程式为:
__________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
重水( 21D2O)是重要的核工业原料,下列说法错误的是( )
A.氘(D)原子核外有1个电子 B.1H与D互称同位素
C.H2O与D2O互称同素异形体 D.1H218O与D216O的相对分子质量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列过程属于“氮的固定”的是 ( )
A.NO2 和H2O反应生成HNO3
B.N2和O2经放电生成NO
C.通过加压、降温等方法将氮气转变为液态氮
D.NH3被H2SO4硫酸吸收生成(NH4)2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
为了测定某气态烃A的化学式,取一定量的A置于一密闭容器中燃烧,实验表明产物是CO2、CO和水蒸气。学生甲、乙设计了两个方案,均认为根据自己的方案能求出A的最简式,他们在一定条件下测得有关数据如下(图中的箭头表示气流的方向,实验前系统内的空气已排尽):
甲方案:燃烧产物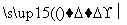 浓硫酸增重2.52 g
浓硫酸增重2.52 g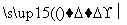
碱石灰增重1.32 g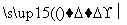 生成CO2 1.76 g
生成CO2 1.76 g
乙方案:燃烧产物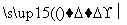 碱石灰增重5.60 g
碱石灰增重5.60 g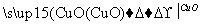
固体减小0.64 g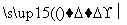 白色沉淀4.00 g
白色沉淀4.00 g
请回答下列问题:
(1)你认为________________(填“甲”或者“乙”)方案能求出A的最简式。
(2)请根据你选择的方案,通过计算求出A的最简式为________。
(3)若要确定A的分子式,________________(填“是”或者“否”)需要测定其他数据,原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:CO(g)+H2O(g)CO2(g)+H2(g) ΔH=Q,其平衡常数随温度变化如下表所示:
| 温度/℃ | 400 | 500 | 850 |
| 平衡常数 | 9.94 | 9 | 1 |
请回答下列问题:
(1)上述反应的化学平衡常数表达式为:________________。该反应的Q________________0(填“>”或“<”)。
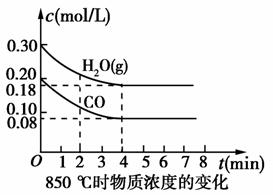
(2)850 ℃时在体积为10 L反应器中,通入一定量的CO和H2O(g),发生上述反应,CO和H2O(g)浓度变化如图所示,则0~4 min时平均反应速率v(CO)=________。
(3)若在500 ℃时进行,且CO、H2O(g)的起始浓度均为0.020 mol/L,该条件下,CO的最大转化率为________________。
(4)若在850 ℃时进行,设起始时CO和H2O(g)共为1 mol,其中水蒸气的体积分数为x,平衡时CO的转化率为y,试推导y随x变化的函数关系式为________________。
(5)某电化学装置可实现2CO2===2CO+O2的转化,使CO重复使用。已知该反应的阳极反应为4OH--4e-===2H2O+O2↑,则阴极反应式为________________。
(6)有人提出可以设计反应2CO===2C+O2(ΔH>0)来消除CO的污染。请判断上述反应能否自发进行:________________(填“可能”或“不可能”),理由是________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com