
ÓŠ¹Ųµ°°×ÖŹµÄŠšŹöÕżČ·µÄŹĒ (””””)
A£®µ°°×ÖŹČÜŅŗÖŠ£¬¼ÓČėÅصÄĮņĖįļ§ČÜŅŗÓŠ³ĮµķĪö³ö£¬¼ÓĖ®ŗó³Įµķ²»Čܽā
B£®µ°°×ÖŹŹōÓŚĢģČ»øß·Ö×Ó»ÆŗĻĪļ
C£®µ°°×ÖŹµÄ·Ö×ÓÄÜĶø¹ż°ėĶøĤ
D£®µ°°×ÖŹøśÅØŃĪĖį×÷ÓĆŹ±³Ź»ĘÉ«
 ĮĮµć¼¤»ī¾«±ąĢįÓÅ100·Ö“óŹŌ¾ķĻµĮŠ“š°ø
ĮĮµć¼¤»ī¾«±ąĢįÓÅ100·Ö“óŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ėę×ÅŹÆÓĶ׏Ō“µÄČÕĒ÷½ōÕÅ£¬ĢģČ»Ęų׏Ō“µÄæŖ·¢ĄūÓƏܵ½Ō½Ą“Ō½¶ąµÄ¹Ų×¢”£ŅŌĢģČ»Ęų(Ö÷ŅŖ³É·ÖŹĒCH4)ĪŖŌĮĻ¾ŗĻ³ÉĘų(Ö÷ŅŖ³É·ÖĪŖCO”¢H2)ÖĘ»Æѧʷ£¬ŹĒÄæĒ°ĢģČ»Ęų×Ŗ»ÆĄūÓƵÄÖ÷ŅŖ¼¼ŹõĀ·Ļß”£¶ų²ÉÓĆŌüÓĶ”¢Ćŗ”¢½¹ĢæĪŖŌĮĻÖĘŗĻ³ÉĘų£¬³£Ņņŗ¬ōŹ»łĢś[Fe(CO)5]µČ¶ųµ¼ÖĀŅŌŗĻ³ÉĘųĪŖŌĮĻŗĻ³É¼×“¼ŗĶŗĻ³É°±µČÉś²ś¹ż³ĢÖŠµÄ“߻ƼĮ²śÉśÖŠ¶¾”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)[Fe(CO)5]ÖŠĢśµÄ»ÆŗĻ¼ŪĪŖ0£¬Š“³öĢśŌ×ӵĻłĢ¬µē×ÓÅŲ¼Ź½£ŗ________________________________________________________________________”£
(2)ÓėCO»„ĪŖµČµē×ÓĢåµÄ·Ö×ÓŗĶĄė×Ó·Ö±šĪŖ________ŗĶ________(ø÷¾ŁŅ»ÖÖ¼“æÉ£¬Ģī»ÆѧŹ½)£¬CO·Ö×ӵĵē×ÓŹ½ĪŖ________£¬CO·Ö×ӵĽį¹¹Ź½æɱķŹ¾³É________”£
(3)ŌŚCH4”¢CO”¢CH3OHÖŠ£¬Ģ¼Ō×Ó²ÉČ”sp3ŌӻƵķÖ×ÓÓŠ________________£¬CH3OHµÄČŪ”¢·Šµć±ČCH4øߣ¬ĘäÖ÷ŅŖŌŅņŹĒ______________________________________”£
(4)CH3CHO·Ö×ÓÖŠ£¬—CH3ÖŠµÄĢ¼Ō×Ó²ÉČ”________ŌӻƷ½Ź½£¬—CHOÖŠµÄĢ¼Ō×Ó²ÉČ”________ŌӻƷ½Ź½”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ(””””)
A£®µŚ¢õA×åÓėµŚ¢÷A×åµÄ¶ĢÖÜĘŚŌŖĖŲµÄŌ×Ӽ乹³ÉµÄĖłÓŠ·Ö×Ó£¬ĘäŌ×Ó¾łĀś×ć×īĶā²ć8µē×Ó½į¹¹
B£®µŚ¢ńA×åŌŖĖŲµ„ÖŹČŪ·ŠµćĖę×ÅŗĖµēŗÉŹżµÄµŻŌö¶ųÉżøß
C£®ŅņĪŖFµÄ·Ē½šŹōŠŌĒæÓŚClµÄ£¬ĖłŅŌHFµÄĖįŠŌĒæÓŚHClµÄ
D£®Ąė×Ó°ė¾¶£ŗr(S2£)£¾r(O2£)£¾r(Na£«)£¾r(Al3£«)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻÖÓŠĘßĘæĪŽ±źĒ©µÄŅŗĢ壬æÉÄÜŹĒ¢ŁŅŅ“¼”¢¢ŚŅŅĖį”¢¢Ū±½”¢¢ÜŅŅĖįŅŅõ„”¢¢ŻÓĶÖ¬”¢¢ŽĘĻĢŃĢĒČÜŅŗ”¢¢ßÕįĢĒČÜŅŗ£¬ĻÖĶعżŅŌĻĀ²½Ö襓ȷ¶Øø÷ŹŌ¼ĮĘæÖŠĖł×°ŅŗĢåµÄĆū³Ę”£
| ŹµŃé²½ÖčŗĶ·½·Ø | ŹµŃéĻÖĻó |
| ¢ń.°Ń7ĘæŅŗĢå·Ö±šŅĄ“Ī±źŗÅA”¢B”¢C”¢D”¢E”¢F”¢GŗóĪÅĘųĢå | Ö»ÓŠF”¢GĮ½ÖÖŅŗĢåƻӊĘųĪ¶ |
| ¢ņ.ø÷ȔɣĮæÓŚŹŌ¹ÜÖŠ¼ÓĖ®Ļ”ŹĶ | Ö»ÓŠC”¢D”¢EČżÖÖŅŗĢå²»Čܽā¶ųø”ŌŚĖ®ÉĻ²ć |
| ¢ó.·Ö±šČ”ÉŁĮæ7ÖÖŅŗĢåÓŚŹŌ¹ÜÖŠ¼ÓŠĀÖʵÄCu(OH)2Šü×ĒŅŗ²¢¼ÓČČ | Ö»ÓŠBŹ¹³ĮµķČܽā£¬FÖŠ²śÉśŗģÉ«³Įµķ |
| ¢ō.ø÷Č”C”¢D”¢EÉŁĮæÓŚŹŌ¹ÜÖŠ£¬¼ÓĻ”NaOHČÜŅŗ²¢¼ÓČČ | Ö»ÓŠCČŌÓŠ·Ö²ćĻÖĻó£¬ĒŅŌŚDµÄŹŌ¹ÜÖŠĪŵ½ĢŲŹāĻćĪ¶ |
øųŹŌ¼ĮĘæÖŲŠĀĢłÉĻ±źĒ©£ŗ
A________ӢB________ӢC________ӢD________ӢE________ӢF________ӢG________ӣ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
½«ĶĮ¶¹ĒŠæŖ£¬Ņ»¶ĪŹ±¼äŗóæɹŪ²ģµ½ĒŠĆę±äĄ¶£¬ĖµĆ÷ĶĮ¶¹ÖŠŗ¬ÓŠ (””””)
A£®µķ·ŪŗĶI£ B£®µķ·ŪŗĶI2
C£®µķ·ŪŗĶKIO3 D£®ĘĻĢŃĢĒŗĶI2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Éś»ī“¦“¦ÓŠ»Æѧ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ(””””)
A£®ÖĘ·¹É×”¢·¹ŗŠ”¢øßŃ¹¹ųµČµÄ²»ŠāøÖŹĒŗĻ½š
B£®×öŅĀ·žµÄĆŽŗĶĀé¾łÓėµķ·Ū»„ĪŖĶ¬·ÖŅģ¹¹Ģå
C£®¼åÕØŹ³ĪļµÄ»ØÉśÓĶŗĶÅ£ÓĶ¶¼ŹĒæÉŌķ»ÆµÄ±„ŗĶõ„Ąą
D£®Ä„¶¹½¬µÄ“ó¶¹ø»ŗ¬µ°°×ÖŹ£¬¶¹½¬Öó·Šŗóµ°°×ÖŹ±ä³ÉĮĖ°±»łĖį
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓĶÖ¬¼ČŹĒÖŲŅŖµÄŹ³Īļ£¬ÓÖŹĒÖŲŅŖµÄ»Æ¹¤ŌĮĻ”£ÓĶÖ¬µÄŅŌĻĀŠŌÖŹŗĶÓĆĶ¾ÓėĘäŗ¬ÓŠµÄ²»±„ŗĶĢ¼Ģ¼Ė«¼üÓŠ¹ŲµÄŹĒ(””””)
A£®ŹŹĮæÉćČėÓĶÖ¬£¬ÓŠÖśÓŚČĖĢåĪüŹÕ¶ąÖÖÖ¬ČÜŠŌĪ¬ÉśĖŲŗĶŗśĀܲ·ĖŲ
B£®ĄūÓĆÓĶÖ¬ŌŚ¼īŠŌĢõ¼žĻĀĖ®½ā£¬æÉŅŌÉś²śøŹÓĶŗĶ·ŹŌķ
C£®Ö²ĪļÓĶĶعżĒā»Æ£¬¼“ÓėĒāĘų·¢Éś¼Ó³É·“Ó¦£¬æÉŅŌÖĘŌģÖ²ĪļÄĢÓĶ(ČĖŌģÄĢÓĶ)
D£®ÓĶ֬ƻӊ¹Ģ¶ØµÄČŪ”¢·Šµć
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŃÖŖŃĒĮņĖįÄĘŌŚæÕĘųÖŠÄܱ»ŃõĘųŃõ»ÆÉś³ÉĮņĖįŃĪ”£
¢ń.¼×Ķ¬Ń§Éč¼ĘĮ½ÖÖ·½°øĄ“¼ģŃéNa2SO3ČÜŅŗŹĒ·ń·¢Éś±äÖŹ”£
·½°øŅ»£ŗȔѳ£¬¼ÓČėĻ”ŃĪĖįÓŠĘųÅŻÉś³É£¬ČĻĪŖŃĒĮņĖįÄĘČÜŅŗƻӊ±äÖŹ”£
·½°ø¶ž£ŗȔѳ£¬¼ÓČėĀČ»Æ±µČÜŅŗÓŠ°×É«³ĮµķÉś³É£¬ČĻĪŖŃĒĮņĖįÄĘČÜŅŗĶźČ«±äÖŹ”£
ĒėÄć¶ŌĮ½·½°ø×÷³öĘĄ¼Ū£ŗ
·½°øŅ»£ŗ________(Ģī”°ŗĻĄķ”±»ņ”°²»ŗĻĄķ”±)£¬ĄķÓÉŹĒ________________________________”£
·½°ø¶ž£ŗ________(Ģī”°ŗĻĄķ”±»ņ”°²»ŗĻĄķ”±)£¬ĄķÓÉŹĒ___________________”£
¢ņ.ŅŅĶ¬Ń§Ģ½¾æNa2SO3ČÜŅŗŹĒ·ń·¢Éś±äÖŹ£¬Éč¼ĘČēĻĀŹµŃé²ā¶Ø1.0 mol·L£1 Na2SO3ČÜŅŗµÄŹµ¼ŹÅØ¶Č”£
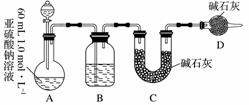
(1)·ÖŅŗĀ©¶·ÖŠÓ¦¼ÓČė×ćĮæµÄĻĀĮŠÄÄÖÖŹŌ¼Į£æ________(Ģī×ÖÄø)
a£®ÅØĻõĖį””””””””b£®65%ĮņĖį””””””””c£®ÅØŃĪĖį
(2)ŹµŃéĒ°ŗó²āµĆC×°ÖĆŌöÖŲ3.2 g£¬ŌņNa2SO3ČÜŅŗŹµ¼ŹµÄĪļÖŹµÄĮæÅضČĪŖ________”£
(3)øĆŹµŃé×°ÖĆ»¹“ęŌŚŅ»øöĆ÷ĻŌµÄȱĻŻŹĒ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĪļÖŹÖŠ£¬¼Čŗ¬ÓŠ¼«ŠŌ¼üÓÖŗ¬ÓŠ·Ē¼«ŠŌ¼üµÄŹĒ (””””)
A. 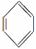 B£®CO2
B£®CO2
C£®Na2O2 D£®NH4Cl
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com