
CuCl2��Һ�е�ͭ��Ҫ��Cu(H2O)42+��CuCl42-��ʽ���ڣ����Ǽ�������ת����ϵ��Cu(H2O)42+(��ɫ)+4Cl- CuCl42-(��ɫ)+4H2O����ⲻͬŨ�ȵ�CuCl2��Һ�����ɿ���Cu2+��Cl-ֱ�ӷŵ硣��ͼΪ���Ũ�Ƚϴ�CuCl2��Һ��װ�ã�ʵ�鿪ʼ�۲쵽���е�KI-������Һ�����������ش��������⣺
CuCl42-(��ɫ)+4H2O����ⲻͬŨ�ȵ�CuCl2��Һ�����ɿ���Cu2+��Cl-ֱ�ӷŵ硣��ͼΪ���Ũ�Ƚϴ�CuCl2��Һ��װ�ã�ʵ�鿪ʼ�۲쵽���е�KI-������Һ�����������ش��������⣺
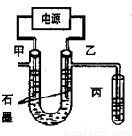
��1���缫�ĵ缫��ӦʽΪ_________________��
��2��������Һ�������ҵ缫������KI��Ӧ���µģ��÷�Ӧ�Ļ�ѧ����ʽΪ___��
��3������IJ��Ͻ��У�U������Һ����ɫ�仯Ϊ__________��
A���ɻ�ɫ��Ϊdz��ɫ B������ɫ��Ϊdz��ɫ
��Һ��ɫ�仯��ԭ����_________________��
��4������һ���̶ȣ��缫����������ɫCu(OH)2��״�����缫������Һ��pH��a����ʱ�缫������Һ��c(Cu2+)��______ mol��L-1������֪��Cu(OH)2��Ksp��2.2��10-20��
��5�����ϳ�ʱ�������Һ����ɫ�ֻ���ȥ��������Ϊ�ҵ缫�����һ����I2����ΪIO3-���÷�Ӧ�����ӷ���ʽΪ_____________��
��1��Cu2++2e-=Cu
��2��Cl2+2KI=2KCl+I2
��3��A ���ŵ���ʱ�У�Cl-�������ģ�CuCl42-ת��ΪCu(H2O)42+
��4��2.2��10��8-2a��
��5��5Cl2+I2+6H2O=10Cl-+2IO3-+12H+
����������1����Ϊ������������ԭ��Ӧ����ͭ���缫����ʽΪCu2++2e-=Cu��
��2��������Һ�������ҵ缫������KI��Ӧ���µģ���Ӧ�ķ���ʽΪ
Cl2+2KI=2KCl+I2��
��3�����ŵ��Ľ��У���Һ��Cl-�������ģ�CuCl42-ת��ΪCu(H2O)42+����Cu��H2O��42+����ɫ��+4Cl-?CuCl42-����ɫ��+4H2O��֪����ҺӦ��Ϊ��ɫ��
��4��Ksp=c2��OH-����c��Cu2+����c��Cu2+��=2.2��10?20/��10a-14��2=2.2��10��8-2a��
��5�����ϳ�ʱ�������Һ����ɫ�ֻ���ȥ��������Ϊ�ҵ缫�����һ����I2����ΪIO3-,˵�������͵��������������ԭ��Ӧ����Ӧ�����ӷ���ʽΪ5Cl2+I2+6H2O=10Cl-+2IO3-+12H+



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��11 ���ͣ�ѡ����
��һ��δ��ɵ����ӷ���ʽ +XO3��+6H+=3X2+3H2O���ݴ��ж�����˵������ȷ����
A��X���������ڱ��еڶ�����Ԫ��
B��XԪ�ص�ԭ�����������7������
C��X2�ǻ�ԭ���H2O����������
D��������3 mol X2��ת��6 mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ��1 ���ͣ�ѡ����
���в������ܴﵽĿ�ĵ���
ѡ�� | Ŀ�� | ���� |
A | ����100 mL 1.0 mol/L CuSO4��Һ | ��25 g CuSO4��5H2O����100 mL����ˮ�� |
B | �����Ȼ�̼��ȡ��ˮ�еĵ� | ���ˮ�м����������Ȼ�̼�������ã���Һ |
C | ����Һ�н�MnO4����ȫת��ΪMn2�� | ������KMnO4��Һ�еμӺ�Fe2+��Һ����ɫ��ʧ |
D | ȷ��NaCl��Һ���Ƿ����Na2CO3 | ȡ������Һ�μ�CaCl2��Һ���۲��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--Ԥ�� ���ͣ�ѡ����
��֪��P4(g)��6Cl2(g)===4PCl3(g)�� ��H��a kJ��mol��1��
P4(g)��10Cl2(g)===4PCl5(g)����H��b kJ��mol��1��
��֪�γɻ��1 mol��ѧ���ų������յ�������Ϊ�û�ѧ���ļ��ܡ�P4������������ṹ��PCl5��P��Cl���ļ���Ϊc kJ��mol��1��PCl3��P��Cl���ļ���Ϊ1.2c kJ��mol��1������������ȷ����
A��P��P���ļ��ܴ���P��Cl���ļ���
B������Cl2(g)��PCl3(g)===PCl5(s)�ķ�Ӧ�Ȧ�H
C��Cl��Cl���ļ���Ϊ(b��a��5.6c)/4 kJ��mol��1
D��P��P���ļ���Ϊ(5a��3b��12c)/8 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�߿���ʦ�Ƽ���ѧ--�����ۺ�4 ���ͣ������
��糧�ŷ������к��ж�������������ȴ�����Ⱦ�������Ⱦ����о������Ը��ƻ���������Ҫ���塣
��1��úȼ�ղ��������������е������SO2��PM2.5�ȣ���ֱ���ŷŵ������У���������Ҫ���������� ����д��ĸ��ţ�
Aˮ�帻Ӫ���� B�ؽ�����Ⱦ C���� D����
��2��������SO2�ķ���ͨ��װ��ʯ��ʯ��Һ������װ�ÿ��Գ�ȥ���еĶ��������ڷ�������Ĺ����У����õ�ʯ��ʯ��Һ�ڽ�������װ��ǰ����ͨһ��ʱ��Ķ�����̼��������������Ч�ʣ�����ʱ���ƽ�Һ��pHֵ����ʱ��Һ���е���������ƿ��Ա���������������������ơ�д����������Ʊ���������������������ƵĻ�ѧ����ʽ ��
��3�����������һ�������ȼҵ��Ʒ������������������ķ����������������£�
A�Ļ�ѧʽ ��������ag A�������Ͽ��Ի���SO2������Ϊ g��
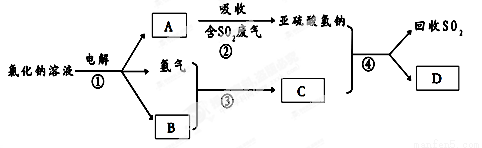
��4������β���к��еĵ������NOx�����γ����꣬д��NO2ת��ΪHNO3�Ļ�ѧ����ʽ ����β���п�������ʱ��NOX�ڴ�ת�����б���ԭ��N2�ų���д��NO��CO��ԭ�Ļ�ѧ����ʽ ��
��5����ҵ�ϳ���Na2CO3��Һ����úȼ�ղ�����������д��SO2��NO��Na2CO3��Һ��Ӧ����Na2SO4��N2�����ӷ���ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014������Ϫһ�С�������ѧ���ݰ�һ�и�һ��ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ������
��13�֣���ѧ�ڻ�������������ʮ����Ҫ�����á������������͵绯ѧ���ⷨ����������ˮ�������ε���Ⱦ��
��1�������������У�H2�ܽ�NO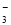 ��ԭΪN2��25��ʱ����Ӧ����10 min����Һ��pH��7��Ϊ12�������£���
��ԭΪN2��25��ʱ����Ӧ����10 min����Һ��pH��7��Ϊ12�������£���
�� ��֪��pH=-lgc(H+),�����£�ˮ��Һ��c(H+)��c(OH-)=10-14 ��
��N2�ĽṹʽΪ________��
���벹�����ӷ���ʽ����������ƽ��������Ӧ���ӷ���ʽΪ(��ƽΪ1��ʡ��)
�� ��NO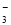 ���� ��H2 ���� �� ��N2���� ��H2O���� ��__________��
���� ��H2 ���� �� ��N2���� ��H2O���� ��__________��
��ƽ����Ӧ����v(NO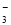 )= mol��L��1��min��1��
)= mol��L��1��min��1��
��2���绯ѧ����NO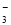 ��ԭ����ͼ��ʾ��
��ԭ����ͼ��ʾ��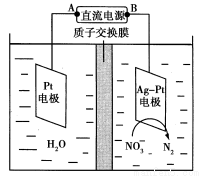
�ٵ�Դ����Ϊ________(�A����B��)��
������ӦʽΪ ��
������������ת����2 mol���ӣ���Ĥ������Һ�������仯��(��m��m��)Ϊ________g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014������Ϫһ�С�������ѧ���ݰ�һ�и�һ��ѧ����ĩ��ѧ�Ծ��������棩 ���ͣ�ѡ����
�ס������ֽ������ʱȽϣ��ټĵ����ۡ��е���ҵĵͣ��ڳ����£�������ˮ��Ӧ�ų��������Ҳ��ܣ�������������Ӧ��ˮ������ԱȽϣ��ұȼ�ǿ���ܼס������缫��ϡ����Ϊ�������Һ���ԭ��أ��ҵ缫����������ݡ�������Ŀ���ܹ�˵���ױ��ҵĽ�����ǿ����( )
A���٢� B. �ڢ� C. �ڢ� D. �٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014���ճ����и߶���ѧ��ĩģ��4������2��ѡ��4���ṹ���Ծ��������棩 ���ͣ������
��12�֣�������Ԫ��A��B��C��D��AԪ�ص�ԭ�����������Ų�Ϊns1��BԪ�ص�ԭ�Ӽ۵����Ų�Ϊns2np2��CԪ�ص�����������������Ӳ�����3����DԪ��ԭ�ӵ�M���Ӳ��P�������3��δ�ɶԵ��ӡ�
��1��Cԭ�ӵĵ����Ų�ʽΪ ����AΪ�ǽ���Ԫ�أ���ԭ�ӹ�����ص���ʽ��A��C�γɵĻ������еĹ��ۼ����� ������ҡ��С�����
��2����n=2ʱ��Bλ��Ԫ�����ڱ��ĵ� ���� �壬BC2���� ���ӣ�����ԡ��Ǽ��ԡ�������n=3ʱ��B��C�γɵľ������� ���塣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��߿���ѧ³�ư�4.1�衡���ǽ���������ϰ���������棩 ���ͣ�ѡ����
��ʯ��(crocidolite)������������֯ȷ�ϵ�һ���°����ʣ��ǡ�¹�ص���Լ���������Ƶ�46�ֻ�ѧƷ֮һ����ʯ�Ļ�ѧʽΪNa2Fe5Si8O22(OH)2����ʯ����ϡ���ᴦ��ʱ����ԭ����ֻ��NO������˵������ȷ����(����)��
A����ʯ����һ����ȼƷ����������ˮ
B����ʯ�Ļ�ѧ��������������ʽ�ɱ�ʾΪ��Na2O��3FeO��Fe2O3��8SiO2��H2O
C��1 mol Na2Fe5Si8O22(OH)2���������������ã�����������8.5 L 2 mol��L��1 HNO3��Һ
D��1 mol Na2Fe5Si8O22(OH)2��������������ã�����������7 L 2 mol��L��1 HF��Һ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com