
【题目】向某硫酸和硫酸铜的混合溶液中加入某浓度的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。下列说法正确的是
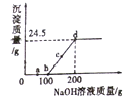
A. a点溶液中含有两种溶质
B. bc段发生反应的类型为置换反应
C. 根据图中数据可计算出氢氧化钠溶液的质量分数
D. d点溶液中主要存在的离子为Na+、Cu2+、OH-、SO42-
科目:高中化学 来源: 题型:
【题目】对于反应:3BrF3+5H2O=Br2+HBrO3+O2+9HF,下列说法正确的是( )
A.该反应中,有三种元素化合价发生改变
B.该反应的氧化剂为BrF3 , 氧化产物为O2
C.1.5molBrF3参加反应,有4mole一转移
D.1.5molH2O参加反应,被H2O还原的BrF3为0.4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两烧杯中各盛有100mL 1.5mol/L的盐酸和氢氧化钠溶液,向两烧杯中加入等质量的铝粉,反应结束后生成气体的体积比为甲:乙=1:2,则加入铝粉的质量为( )
A.1.8g
B.3.6g
C.2.7g
D.5.4g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前,林芝市已进入雨季,空气质量优良,PM2.5<100。下列物质中不列入首要污染物的是( )
A. 可吸入颗粒物B. NO2C. SO2D. CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛.回答下列问题:
(1)基态Ge原子的核外电子排布式为[Ar] , 有个未成对电子.
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键.从原子结构角度分析,原因是 .
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因
GeCl4 | GeBr4 | GeI4 | |
熔点/℃ | ﹣49.5 | 26 | 146 |
沸点/℃ | 83.1 | 186 | 约400 |
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂.Zn、Ge、O电负性由大至小的顺序是 .
(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为 , 微粒之间存在的作用力是 .
(6)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为( ![]() ,0,
,0, ![]() ),C为(
),C为( ![]() ,
, ![]() ,0).则D原子的坐标参数为 .
,0).则D原子的坐标参数为 .
②晶胞参数,描述晶胞的大小和形状,已知Ge单晶的晶胞参数a=565.76pm,其密度为gcm﹣3(列出计算式即可).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学化学中的一些常见物质有如图转化关系(部分产物未给出).其中A、H的焰色呈黄色,D常温下为黄绿色气体,反应③为侯氏制碱法反应原理之一,E是常见的金属.
回答下列问题.
(1)D的电子式为 .
(2)H的化学式为 .
(3)写出反应①的化学方程式 .
(4)写出反应②的离子方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com