
下列说法正确的是(NA为阿伏加罗常数)
A.1molP4含有P-P键的个数为4NA
B.7.8g 过氧化钠含有的共用电子对数为0.2NA
C.1mol金刚石中含有C-C键的个数为2NA
D.1molSiO2中含Si-O键的个数为2NA
科目:高中化学 来源:2015-2016学年浙江省高一下期末化学试卷(解析版) 题型:实验题
实
 验室制乙酸乙酯得主要
验室制乙酸乙酯得主要 装置如图中A所示,主要步骤:
装置如图中A所示,主要步骤:
①在a试管中按2∶3∶2的体积比配制浓硫酸、乙醇、乙酸的混合物;
②按A图连接装置,使产生的蒸气经导管通到b试管所盛的饱和碳酸钠溶液(加入几滴酚酞试液)中;
③小火加热a试管中的混合液;
④等b试管中收集到约2 mL产物时停止加热。撤下b试管并用力振荡,然后静置待其中液体分层;
⑤分离出纯净的乙酸乙酯。
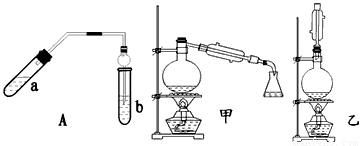
请回答下列问题:
(1)步骤④中可观察到b试管中有细小的气泡冒出,写出该反应的离子方程式:________。
(2)A装置中使用球形管除起到冷凝作用外,另一重要作用是_____________________;步骤⑤中分离乙酸乙酯必须使用的一种仪器是_______________________________。
(3)为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图A所示装置进行了以下4个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡小试管b再测有机层的厚度,实验记录如下:
实验编号 | 试管a中试剂 | 试管b中试剂 | 测得有机层的厚度/cm |
A | 3 mL乙醇、2 mL乙酸、1mL18mol·L-1 浓硫酸 | 饱和Na2CO3溶液 | 5.0 |
B | 3 mL乙醇、2 mL乙酸 | 0.1 | |
C | 3 mL乙醇、2 mL乙酸、6 mL 3mol·L-1 H2SO4 | 1.2 | |
D | 3 mL乙醇、2 mL乙酸、盐酸 | 1.2 |
① 实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是________mL和________mol·L-1 。
② 分析实验________(填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率。
③ 加热有利于提高乙酸乙酯的产率,但实验发现温度过高乙酸乙酯的产率反而降低,可能的原因是 。
④为充分利用反应物,该同学又设计了图中甲、乙两个装置(利用乙装置时,待反应完毕冷却后,再用饱和碳酸钠溶液提取烧瓶中的产物)。你认为更合理的是______。理由是:____________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川成都外国语学校高一下期末文科化学卷(解析版) 题型:选择题
在一定温度下,可逆反应A(气)+3B(气)  2C(气)达到平衡
2C(气)达到平衡 的标志是
的标志是
A.C生成的速率与C分解的速率相等
B.A、B、C的浓度相等
C.A、 B、C的分子数比为1:3:2
B、C的分子数比为1:3:2
D.单位时间生成n mol A,同时生成3n mol B
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆乌鲁木齐七十中高二下期末化学试卷(解析版) 题型:实验题
已知某纯碱样品中含有NaCl杂质,为测定样品中纯碱的质量分数,甲同学用下图装置及试剂进行实验(夹持仪器略).
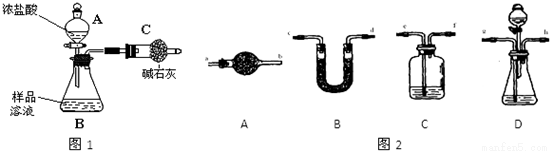
(1)仪器A的名称分别是____________________________________;
(2)甲同学按实验正常操作的主要步骤如下:
①按图组装好仪器后,______________________检查装置气密性,连接好装置
;
②将ag试样放入仪器B中,加适量蒸馏水溶解,得到样品溶液;
③称量盛有碱石灰的干燥管的质量为bg;
④从仪器A中滴入浓盐酸,直到不再产生气体时为止;
⑤再次称量盛有碱石灰的干燥管的质量为cg;
(3)甲同学根据以上实验求得的样品中Na2CO3的质量分数是____________
(用含a、b、c的式子表示).
(4)乙同学认为甲同学在实验装置设计和使用药品上都有缺陷,会导致测得的Na2CO3的质量分数偏高,而丙同学则认为甲同学的实验装置会使测得的结果偏低,丙同学认为结果偏低的原因是______________;
(5)若要解决乙、丙同学指出的甲同学实验中的问题,可对甲同学的实验装置和实验药品进行适当的改动,请按合理顺序选择如图2所示仪器并完成下表:(从e口鼓入空气,D中锥形瓶中装入样品溶液,用大写字母代表仪器,仪器可重复使用,夹持仪器略)
选用的仪器 | D | A | |||
添加的药品 | 分液漏斗中药品__________ |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆乌鲁木齐七十中高二下期末化学试卷(解析版) 题型:选择题
下列说法正确的是
A.乙醇中的-OH上的氢比水分子的一个-OH上的氢活泼
B.[TiCl(H2O)5]Cl2·H2O的配合物内界和外界Cl-的数目比是1:2
C.酸性:H3PO4<H3PO3
D.手性分子CH2=CH(CH2OH)COOH与足量的H2反应后分子有两个手性碳原子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆乌鲁木齐七十中高二下期末化学试卷(解析版) 题型:选择题
下列各组物质相互混合反应后,既有气体生成,最终又有沉淀生成的是
①金属钠投入到FeCl3溶液中
②过量NaOH溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中
④Na2O2投入FeCl2溶液中
A.只有③ B.只有①④ C.只有②③ D.只有①③④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆乌鲁木齐七十中高二下期末化学试卷(解析版) 题型:选择题
下列关于晶体的说法中,不正确的是
①晶体中原子呈周期性有序排列,有自范性;而非晶体中原子排列相对无序,无自范性
②含有金属阳离子的晶体一定是离子晶体
③共价键可决定分子晶体的熔、沸点
④在分子晶体中一定不存在离子键,而在离子晶体中可能存在共价键
⑤晶胞是晶体结构的基本单元,晶体内部的微粒按一定规律作周期性重复排列
⑥晶体尽可能采取紧密堆积方式,以使其变得比较稳定
⑦干冰晶体中,一个CO2分子周围有12个CO2分子紧邻
A.①②③ B.②③ C.④⑤⑥ D.②③④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二下期末化学试卷(解析版) 题型:选择题
向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液。下列对此现象说法正确的是( )
A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变
B.沉淀溶解后,将生成深蓝色的配合离子[Cu(NH3)4] 2+
C.上述现象说明[Cu(NH3)4] 2+不如Cu(OH)2稳定
D.在[Cu(NH3)4] 2+离子中,Cu2+给出孤电子对,NH3提 供空轨道
供空轨道
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com