
| A.一定是O2与NO2的混合气体 | B.可能是NO和NO2的混合气体 |
| C.可能是N2与NO2的混合气体 | D.只可能是NO2一种气体 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
A.Cu Cu(NO3)2 Cu(NO3)2 | B.Cu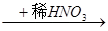 Cu(NO3)2 Cu(NO3)2 |
C.Cu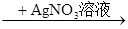 Cu(NO3)2 Cu(NO3)2 | D.Cu  CuO CuO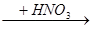 Cu(NO3)2 Cu(NO3)2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
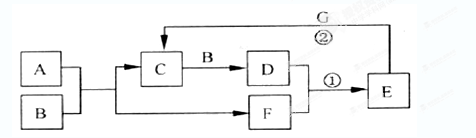
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
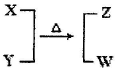
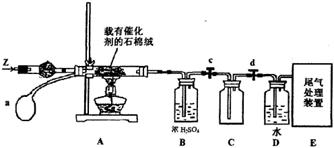
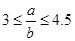 ,则被还原的HNO3的质量为 g。
,则被还原的HNO3的质量为 g。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NH3、NO | B.NO2、NO | C.NH3、NO2 | D.NO、NO2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
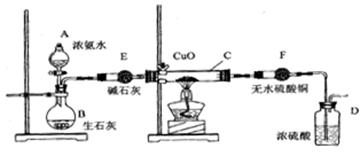
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
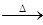 2M+2NO2↑+O2↑,加热3.40gMNO3,生成NO2和O2折算成标准状况时的总体积为672mL。由此可以计算出M的相对原子质量为_____________。
2M+2NO2↑+O2↑,加热3.40gMNO3,生成NO2和O2折算成标准状况时的总体积为672mL。由此可以计算出M的相对原子质量为_____________。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
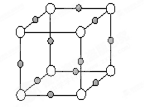
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com