
元素H、C、N、O、F都是重要的非金属元素,Fe、Cu是应用非常广泛的金属。
(1)Fe元素基态原子的核外电子排布式为 。
(2)C、H元素形成的化合物分子中共有16个电子,该分子中σ键与π键的个数比为
(3)C、N、O三种元素的第一电离能由大到小的顺序为(用元素符号表示)
(4)在测定HF的相对分子质量时,实验测得值一般高于理论值,其主要原因是
(5)C、N两元素形成的化合物C3N4形成的原子晶体,结构类似金刚石,甚至硬度超过金刚石,其原因是
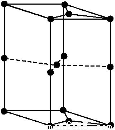
(6)如图为石墨晶胞结构示意图,该晶胞中含有碳原子的个数为
(1)1s22s22p63s23p63d64s2
(2)5∶1 (3)N>O>C
(4)HF分子间存在氢键,易形成缔合分子(HF)n
(5)氮原子半径小于碳原子半径,氮碳形成的共价键键长比碳碳键键长短,键能更大,所以C3N4硬度更大
(6)4
【解析】(1)铁是26号元素,其核外电子排布式为1s22s22p63s23p63d64s2。
(2)C、H元素形成的化合物分子中共有16个电子的物质是CH2 CH2,单键全是σ键,双键中有1个π键和1个σ键,故σ键与π键的个数比为5∶1。
CH2,单键全是σ键,双键中有1个π键和1个σ键,故σ键与π键的个数比为5∶1。
(3)同一周期从左往右,第一电离能有逐渐增大趋势,且前四周期中ⅤA元素第一电离能比相邻元素大,故C、N、O三种元素的第一电离能由大到小的顺序为N>O>C。
(4)HF分子之间能形成氢键使分子缔合在一起,所以测得的相对分子质量为缔合分子的相对分子质量,故实验测得值一般高于理论值。
(5)原子晶体的硬度大小与共价键的强弱有关,共价键键长越短硬度越大,因氮原子半径小于碳原子半径,故C3N4晶体的硬度大于金刚石的硬度。
(6)顶点为8个晶胞所共有,棱上为4个晶胞所共有,面心为2个晶胞所共有,体内为晶胞所独有,石墨晶胞中含有碳原子的个数=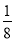 ×8+
×8+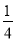 ×4+
×4+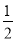 ×2+1×1=4。
×2+1×1=4。


科目:高中化学 来源:2014高考化学名师选择题专练 化学反应中的能量变化练习卷(解析版) 题型:选择题
胶状液氢(主要成分是H2和CH4)有望用于未来的运载火箭和空间运输系统。实验测得101 kPa时,1 mol H2完全燃烧生成液态水,放出285.8 kJ的热量;1 mol CH4完全燃烧生成液态水和CO2气体,放出890.3 kJ的热量。下列热化学方程式书写正确的是( )
A.2H2(g)+O2(g)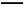 2H2O(l) ΔH=-285.8 kJ/mol
2H2O(l) ΔH=-285.8 kJ/mol
B.CH4(g)+2O2(g)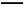 CO2(g)+2H2O(l)ΔH=-890.3 kJ/mol
CO2(g)+2H2O(l)ΔH=-890.3 kJ/mol
C.CH4(g)+2O2(g)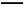 CO2(g)+2H2O(g)ΔH=-890.3 kJ/mol
CO2(g)+2H2O(g)ΔH=-890.3 kJ/mol
D.CH4(g)+2O2(g)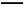 CO2(g)+2H2O(l)ΔH=+890.3 kJ/mol
CO2(g)+2H2O(l)ΔH=+890.3 kJ/mol
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师综合题专练 物质结构与性质练习卷(解析版) 题型:填空题
已知:A、B、C、D、E、F是周期表中前36号元素,A是原子半径最小的元素,B元素基态原子的2p轨道上只有两个电子,C元素的基态原子L层只有2对成对电子,D是元素周期表中电负性最大的元素,E2+的核外电子排布和Ar原子相同,F的核电荷数是D和E的核电荷数之和。
请回答下列问题:
(1)分子式为BC2的空间构型为 形;F2+的核外电子排布式为 。
(2)A分别与B、C形成的最简单化合物的稳定性B C(填“大于”或“小于”);A、C两元素可组成原子个数比为1∶1 的化合物,C元素的杂化类型为 。
(3)A2C所形成的晶体类型为 ;F单质形成的晶体类型为 。
(4)F元素氧化物的熔点比其硫化物的 (填“高”或“低”),请解释其原因
。
(5)E元素与C元素形成的化合物是 化合物,其晶体熔化时破坏的作用力是 ,晶体EC的熔点比晶体BC2的熔点 (填“高”或“低”)。
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师综合题专练 化学实验练习卷(解析版) 题型:实验题
某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。
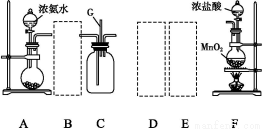
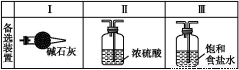
(1)装置F中发生反应的离子方程式为 。
(2)装置A中的烧瓶内固体可选用 (填以下选项的代号)。
A.碱石灰 B.生石灰 C.二氧化硅 D.五氧化二磷 E.烧碱
(3)虚线框内应添加必要的除杂装置,请从上图的备选装置中选择,并将编号填入下列空格:B ,D ,E (均填编号)。
(4)氯气和氨气在常温下相混就会反应生成氯化铵和氮气,装置C内出现浓厚的白烟并在容器内壁凝结,请设计实验方案鉴定该固体就是氯化铵: 。
(5)从装置C的出气管口处逸出的尾气可能含有污染环境的气体,如何处理?
。
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师综合题专练 化学反应原理练习卷(解析版) 题型:填空题
Ⅰ.铝是地壳中含量最高的金属元素,其单质及其合金在生产生活中的应用十分广泛。
(1)金属铝的生产是以Al2O3为原料,与冰晶石(Na3AlF6)在熔融状态下进行电解,则化学方程式为 。
其电极均由石墨材料做成,则电解时不断消耗的电极是 (填“阴极”或“阳极”)。
(2)对铝制品进行抗腐蚀处理,可延长其使用寿命。以处理过的铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极反应式为 。
(3)铝电池性能优越,Al-Ag2O电池可用作水下动力电源,化学反应为:2Al+3Ag2O+2NaOH+3H2O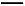 2Na[Al(OH)4]+6Ag, 则负极的电极反应式为
2Na[Al(OH)4]+6Ag, 则负极的电极反应式为
,正极附近溶液的pH (填“变大”、“不变”或“变小”)。
Ⅱ.氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
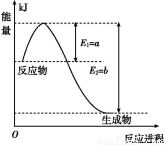
(1)如图是在一定温度和压强下N2和H2反应生成1 mol NH3过程中能量变化示意图,请写出合成氨的热化学反应方程式: (ΔH的数值用含字母a、b的代数式表示)。
(2)工业合成氨的反应为N2(g)+3H2(g) 2NH3(g)。在一定温度下,将一定量的N2和H2通入体积为1 L的密闭容器中,反应达到平衡后,改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是 。
2NH3(g)。在一定温度下,将一定量的N2和H2通入体积为1 L的密闭容器中,反应达到平衡后,改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是 。
A.增大压强 B.增大反应物的浓度
C.使用催化剂 D.降低温度
Ⅲ.铁及其化合物在生活、生产中有广泛应用。请回答下列问题:黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为:3FeS2+8O2 6SO2+Fe3O4,有3 mol FeS2参加反应,转移 mol电子。
6SO2+Fe3O4,有3 mol FeS2参加反应,转移 mol电子。
(2)氯化铁溶液称为化学试剂中的“多面手”,写出SO2通入氯化铁溶液中反应的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 选修3物质结构与性质练习卷(解析版) 题型:选择题
PH3是一种无色剧毒气体,其分子结构和NH3相似,但P-H键键能比N-H键键能低。下列判断中错误的是( )
A.PH3分子呈三角锥形
B.PH3分子是极性分子
C.PH3沸点低于NH3沸点,因为P—H键键能低
D.PH3分子稳定性低于NH3分子,因为N—H键键能高
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 选修2化学与技术练习卷(解析版) 题型:选择题
下列说法不正确的是( )
A.使用可再生资源、用超临界二氧化碳替代有机溶剂、注重原子的经济性、采用低能耗生产工艺都符合绿色化学的思想
B.氨基酸是人体必需的营养物质,其晶体主要以内盐形式存在,调节溶液的pH可改变它的溶解度
C.石油裂解、煤的气化、橡胶老化、海水制镁、纯碱晶体风化、纤维素制火棉等过程中都包含化学变化
D.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,也称为“细颗粒物”,PM2.5在空气中只形成气溶胶
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题9溶液中的电离平衡练习卷(解析版) 题型:选择题
针对0.1 mol·L-1的醋酸溶液,下列分析判断正确的是( )
A.升高温度,溶液的pH会增大
B.加入少量固体NaOH,溶液中c(CH3COO-)+c(OH-)>c(Na+)+c(H+)
C.加入少量0.2 mol·L-1的硫酸溶液,水电离产生的c(H+)减小
D.与0.1 mol·L-1的NaOH溶液等体积混合后,溶液中c(CH3COO-)=c(Na+)
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题6原子结构化学键练习卷(解析版) 题型:选择题
据报道,2012年俄罗斯科学家再次合成117号元素。本次实验生成了6个新原子,其中5个 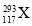 ,1个
,1个 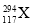 。下列关于
。下列关于 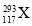 和
和 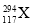 的说法不正确的是( )
的说法不正确的是( )
A.是两种核素 B.互为同位素 C.中子数分别为176和177 D.电子数相差1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com