
��ԭ�����ɷ֣������������SO2��7%��O2��11%��N2��82%��ѹǿ��0.1Mpa��
�¶�/�� | 400 | 450 | 500 | 525 | 550 | 575 | 600 | 650 | 1 000 |
ת����/�� | 99.2 | 97.5 | 95.8 | 93.5 | 90.5 | 85.6 | 79.9 | 73.7 | 58.5 |
SO2�Ӵ�������һ�����ȷ�Ӧ�����ݻ�ѧƽ�������жϣ��˷�Ӧ���¶Ƚϵ͵���������Ϊ��������Ϊʲôʵ�������У�ѡ��400��500 ����Ϊ�����¶�?
(2)ѹǿ��SO2ƽ��ת���ʵ�Ӱ����йز������±���ԭ�����ɷ�ͬ�ڣ�1�����
ѹǿ��Mpa ת����/�� �¶�/�� | 0.1 | 0.5 | 1 | 10 |
400 | 99.2 | 99.6 | 99.7 | 99.9 |
500 | 93.5 | 96.9 | 97.8 | 99.3 |
600 | 73.7 | 85.8 | 89.5 | 96.4 |
���ݻ�ѧƽ�����ۣ������ۺϾ���Ч�棬��ϱ������ݣ������ش�ΪʲôSO2�Ӵ������ڳ�ѹ�½��С�
 ��˼ά������ҵ���ټ��ִ�ѧ������ϵ�д�
��˼ά������ҵ���ټ��ִ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| 1 |
| 2 |
| ���� |
| �� |
| T/K | 673 | 723 | 823 | 923 |
| K | 423 | 37.4 | 20.5 | 4.68 |
| CO |
| ���� |
| ϡ���� |
| ϡ���� |
| ��м |
| ���� |
| ���� |
| ϡ���� |
| H2 |
| ���� |
| ����ͭ��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �¶ȣ��棩 | 25 | t1 | t2 |
| ˮ�����ӻ����� | 1��10-14 | �� | 1��10-13 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �¶�/�� | 25 | t1 | t2 |
| ˮ�����ӻ����� | 1��10-14 | KW | 1��10-12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���߿������С�����ѧ ���ͣ�043
(1)�±��Dz�ͬ�¶���SO2��ƽ��ת���ʣ�[ԭ�����ɷ�(�������)��SO2 7����O2 11����N2 82����ѹǿ��0.1MPa]

SO2�Ӵ�������һ�����ȷ�Ӧ�����ݻ�ѧƽ�������жϣ��˷�Ӧ���¶Ƚϵ͵������½�����Ϊ��������Ϊʲôʵ�������У�ѡ��400�桫500����Ϊ�����¶ȣ�
(2)ѹǿ��SO2ƽ��ת���ʵ�Ӱ��[ԭ�����ɷ�ͬ��(1)��]
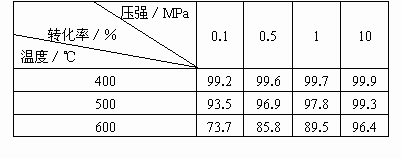
���ݻ�ѧƽ�����ۣ������ۺϾ���Ч�棬��ϱ������ݣ������ش�ΪʲôSO2�Ӵ������ڳ�ѹ�½��У�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com