
2011��3�£��ձ�����9�����𣬵���������Х�������������ؽ����ٶ������ѣ�������ˮ��ȫ����Ҫ����֮һ�����������һ����Ҫ����ɫ��ˮ�������о�ˮ������˫�ع��ܡ�ij����ѧϰС��������·����Ʊ�������أ�
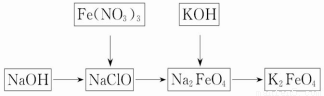
��1�������������Ԫ�صĻ��ϼ�Ϊ_______�ۣ��Ʋ������еĻ�ѧ������____ __��
��2���ڴ�������(NaClO��84����Һ����Ҫ�ɷ�)��Һ�м����ռ�����γɼ��Ի���������ĥ��������������εؼ��뵽������Һ�У���ԡ�з�Ӧ1h�����������ӷ�ӦΪ2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O����������________����KOH���뵽��Ӧ�����Һ�����Сʱ�����ã����˴ֲ�Ʒ���÷�Ӧ�Ļ�ѧ����ʽΪ2KOH+Na2FeO4====K2FeO4+2NaOH�����ݸ��ֽⷴӦԭ�����������Ƶ��ܽ��________������ص��ܽ��(����ڡ�����С�ڡ����ڡ�)��
��3����ǿ������Һ�У���������ܽ��Ǹ�����(KCrO2)����Ϊ������(K2CrO4)�����ɵĸ�������Һ�ữ�õ����ظ����(K2Cr2O7)��Fe(��)�ı���Һ�ζ����Զ�����������Ϊָʾ��������ζ��յ�ʱ����Һ����ɫ��Ϊ����ɫ(+6�۸�ת����+3�۸�)���й����ӷ���ʽΪFeO42-+CrO2-+2H2O====CrO42-+Fe(OH)3��+OH-��2CrO42-+2H+====Cr2O72-+H2O��Cr2O72-+6Fe2++14H+====2Cr3++6Fe3++7H2O
�ֳ�ȡ5.00 g���������Ʒ���ձ��У�������������������Һ�������Թ�����KCrO2����ַ�Ӧ��ת�Ƶ�250 mL����ƿ�У����ݣ���ȡ25.00 mL������ϡ�����ữ����0.100 0 mol��L-1��(NH4)2Fe(SO4)2����Һ�ζ�����ȥ����Һ30.00 mL����������ʵ���Ƶõ���Ʒ�У�������ص���������Ϊ__________��
��10�֣���1��+6 ǿ������ ��2���������� ���� ��3��39.6%
��������
�����������1��������صĻ�ѧʽΪK2FeO4�����ݻ�ѧʽ�л��ϼ۵Ĵ�����Ϊ0�ɵ�FeԪ�صĻ��ϼ�Ϊ+6�����������FeԪ�ش�����ۣ��������ؾ���ǿ�����ԡ�
��2������2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O�л��ϼ۵ı仯��ClO?��ClԪ����+1�۽���ΪCl?�еġ�1�ۣ�����������Ϊ�������ƣ����ݸ��ֽⷴӦԭ������Ӧ������ܵķ�����У�2KOH+Na2FeO4=K2FeO4+2NaOH�����Ը������Ƶ��ܽ�ȴ��ڸ�����ص��ܽ�ȡ�
��3���������ӷ���ʽFeO42-+CrO2-+2H2O=CrO42-+Fe(OH)3��+OH-��2CrO42-+2H+=Cr2O72-+H2O��Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O�ɵö�Ӧ��ϵ��2FeO42?��2CrO2-��Cr2O72?��6Fe3+���ɵ�FeO42?��3Fe2+����25.00 mL ��Һ��n��FeO42?��=1/3n��Fe2+��=1/3��0.100 0 mol��L-1��0.03L=0.001mol����25oml�к�FeO42?���ʵ���Ϊ0.01mol�����Ը�����ص���������=0.01mol��198g/mol��5g��100%=39.6%��
���㣺���⿼��������ԭ��Ӧԭ�������ֽⷴӦ����ѧ���㡣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015�����������и�����ѧ�ڵ�һ��ģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���и������ӣ�����ָ����Һ�й������
����ɫ��Һ�У�K����Cl����Na����HCO3����OH��
�� ʹpH��ֽ������ɫ����Һ�У� K����CO32����Na����AlO2��
��ˮ�����c(H��)=10��12mol��L��1����Һ�У�ClO����HCO3����NO3����NH4����SO32��
�ܼ���Mg�ܷų�H2����Һ�У�Mg2����NH4����Cl����Na����SO42��
��ʹ���ȱ�����Һ�У�MnO4����NO3����SO42����Na����Fe3��
��pH=0����Һ�У�Fe2����Al3����NO3����Cl����SO32��
�٢� B���ڢܢ� C���٢ڢ� D���ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�츣��ʡ�߶���ѧ�ڵڶ����¿���ѧ�Ծ��������棩 ���ͣ������
��16�֣� ��֪2A2��g����B2��g�� 2C3��g������H ����a kJ/mol��a��0������һ���д����Ĺ̶��ݻ��������м���2 mol A2��1 mol B2����500 ��ʱ��ַ�Ӧ��ƽ���C3��Ũ��Ϊw mol/L���ų�����b kJ��
2C3��g������H ����a kJ/mol��a��0������һ���д����Ĺ̶��ݻ��������м���2 mol A2��1 mol B2����500 ��ʱ��ַ�Ӧ��ƽ���C3��Ũ��Ϊw mol/L���ų�����b kJ��
��1���Ƚ�a b�����������������
��2��������Ӧ�¶����ߵ�700�棬�÷�Ӧ��ƽ�ⳣ���� ���������С�����䡱����������Ӧ���������ѹ����ƽ���� �����ƶ��������Ӧ�����淴Ӧ�������÷�Ӧ��ƽ�ⳣ���� �����������С�����䡱��
��3������ԭ���������У�ֻ����2 mol C3��500 ��ʱ��ַ�Ӧ��ƽ�����������ckJ��C3��Ũ��Ҳ��w mol/L����c ���� ����a��b��ʾ����
��4����˵���÷�Ӧ�Ѿ��ﵽƽ��״̬����
A 2v�棨A2����v����B2�� B v����C3����2v����B2��
C A2��C3Ũ����� D����������ƽ����Է�����������
E��������ѹǿ���ֲ��� F���������ܶȱ��ֲ���
��5��Ϊʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����__________��
A����ʱ�����C3���� B���ʵ������¶�
C������B2��Ũ�� D��ѡ���Ч�Ĵ���
��6����������������Ϊ��ѹ��������Ӧǰ�����ͬ������ʼʱ����2 mol A2��1molB2��500 ��ʱ��ַ�Ӧ��ƽ��ų�����dkJ����d b�����������������
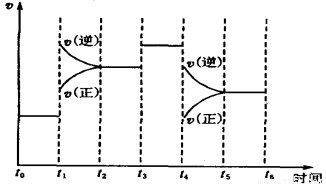
��7����ͼ��ʾ�˷�Ӧ�ķ�Ӧ����v��ʱ��t�Ĺ�ϵͼ��
������ͼ�жϣ���t1��t4ʱ�̸ı����������ֱ��� �� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�츣��ʡ�߶���ѧ�ڵڶ����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�跴ӦC��s����CO2��g�� 2CO��g��������Ӧ���ȣ�������Ӧ����Ϊv1��N2(g)+3H2(g)
2CO��g��������Ӧ���ȣ�������Ӧ����Ϊv1��N2(g)+3H2(g) 2NH3(g)������Ӧ���ȣ�������Ӧ����Ϊv2������������Ӧ�����¶�����ʱ��v1��v2�ı仯���Ϊ �� ��
2NH3(g)������Ӧ���ȣ�������Ӧ����Ϊv2������������Ӧ�����¶�����ʱ��v1��v2�ı仯���Ϊ �� ��
A��v1����v2��С B��ͬʱ��С C��ͬʱ���� D��v1��С��v2����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�츣��ʡ�߶���ѧ�ڵڶ����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���淴ӦA+3B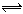 2C+2D,��4�ֲ�ͬ����µķ�Ӧ���ʷֱ�Ϊ��λmol��L��1��s��1��
2C+2D,��4�ֲ�ͬ����µķ�Ӧ���ʷֱ�Ϊ��λmol��L��1��s��1��
��VA=0.20����VB=0.60 ����VD=0.50���� VC=0.45���÷�Ӧ���������� �� ��
A���� B���� C���ٺ͢� D���ں͢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�츣��ʡ������ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ʵ��������2.0 mol/L��Na2CO3��Һ950 mL������ʱӦѡ������ƿ�Ĺ��ͳ�ȡNa2CO3����������ֱ�Ϊ
A��950 mL��201.4 g B��500 mL��100.7 g
C��1000 mL��201.4 g D��1 000 mL��212.0 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�츣��ʡ������ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���ڷ�Ӧ��KHCO3��Һ��ʯ��ˮ��Ӧ;��Na2CO3 ��Һ��ϡ���ᷴӦ;��Na���ռ���Һ��Ӧ;��Fe��ϡ���ᷴӦ;�ı䷴Ӧ��������Ũ��,������ͬһ�����ӷ���ʽ��ʾ����
A���٢ڢ� B���٢ۢ� C���٢ڢ� D���ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�츣��ʡ������ѧ�ڵڶ���������黯ѧ�Ծ��������棩 ���ͣ�ѡ����
������о���Ա������һ�ִ�����Ũ����ȩ��ˮ���·�������Ĥ��ⷨ����ȩ�ֱ�����������������Ӧ��ת��Ϊ�Ҵ������ᡣʵ������һ��Ũ�ȵ���ȩ��Na2SO4��ҺΪ�������Һ��ģ����ȩ��ˮ�Ĵ������̣���װ������ͼ��ʾ������˵������ȷ����
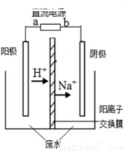
A������CH4������ȼ�ϵ��Ϊֱ����Դ��ȼ�ϵ�ص�a��Ӧͨ�����
B��������ӦCH3CHO -2e- + H2O = CH3COOH +2H+
C���������У�������Na2SO4�����ʵ�������
D���������У��������ֱ�����������Ҵ��⣬����������ɫ���壬��������������O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�츣��ʡ�����и�����ѧ�ڵ������ʼ����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��E��F�����ܱ������У���һ�������·�����Ӧ��E(g)+F(s) 2G(g)�����Թ��������ƽ��ʱG���������(%)���¶Ⱥ�ѹǿ�ı仯���±���ʾ��
2G(g)�����Թ��������ƽ��ʱG���������(%)���¶Ⱥ�ѹǿ�ı仯���±���ʾ��

��b��f ��915�桢2.0MPaʱE��ת����Ϊ60% �۸÷�Ӧ�ġ�S��0 ��K(1000��)��K(810��)��������~������ȷ����
A��4�� B��3�� C��2�� D��1��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com