
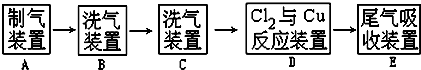
分析 实验室用浓盐酸和二氧化锰加热制取氯气,因为浓盐酸具有挥发性,所以得到的氯气中含有HCl,可在C中用饱和是食盐水除去氯气中的HCl,然后在C装置中用浓硫酸干燥氯气得到较纯净、干燥的氯气,D中氯气和Cu在点燃条件下反应生成氯化铜,因为氯气有毒,则不能直接排空,应该用碱液处理尾气,也可用还原性溶液吸收氯气,以此解答该题.
解答 解:实验室用浓盐酸和二氧化锰加热制取氯气,因为浓盐酸具有挥发性,所以得到的氯气中含有HCl,可在C中用饱和是食盐水除去氯气中的HCl,然后在C装置中用浓硫酸干燥氯气得到较纯净、干燥的氯气,D中氯气和Cu在点燃条件下反应生成氯化铜,因为氯气有毒,则不能直接排空,应该进行处理尾气,
(1)加入条件下浓盐酸与二氧化锰发生氧化还原反应生成氯气,反应的方程式为4HCl(浓)+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑,
故答案为:4HCl(浓)+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+2H2O+Cl2↑;
(2)浓盐酸有挥发性,浓盐酸中的水在加热条件下变成水蒸气,所以氯气中混有氯化氢和水蒸气;氯化氢极易溶于水,氯气能溶于水,且与水反应,Cl2+H2O=H++Cl-+HClO,食盐水溶液中的氯离子抑制氯气的溶解,降低氯气的溶解度,所以可用饱和的食盐水除去HCl气体.
故答案为:饱和食盐水;吸收氯化氢;
(3)加热条件下,氯气和铜反应生成氯化铜,也可用点燃的方法,方程式为Cu+Cl2$\frac{\underline{\;\;△\;\;}}{\;}$ CuCl2,故答案为:Cu+Cl2$\frac{\underline{\;\;△\;\;}}{\;}$ CuCl2;
(4)FeCl2溶液、纯水、KMnO4溶液、稀盐酸、浓硫酸中只有FeCl2溶液与氯气发生反应而达到吸收氯气的作用,反应的离子方程式为2Fe2++Cl2═2Fe3++2Cl-,
故答案为:FeCl2溶液;2Fe2++Cl2═2Fe3++2Cl-.
点评 本题考查物质制备,为高频考点,涉及实验室和工业制取氯气,明确实验原理、物质性质是解本题关键,侧重考查学生实验设计、实验分析能力,知道流程图中气体成分及发生的反应,题目难度不大.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氟酸存放在带橡皮塞的棕色试剂瓶中 | |
| B. | Ca(OH)2溶液存在配磨口玻璃塞的棕色试剂瓶中 | |
| C. | NaOH溶液存放在带橡皮塞的细口玻璃瓶中 | |
| D. | NaOH固体盛放在带橡皮塞的细口玻璃瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
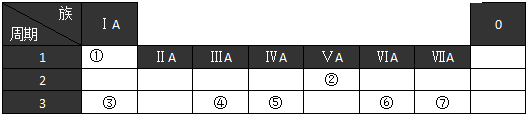
| A. | 它们的氧化物都能与水反应生成对应的酸 | |
| B. | 碳和硅的最高正价都是+4价 | |
| C. | 硅元素在地壳中的含量占第二位,碳占第一位 | |
| D. | 碳和硅在自然界存在形式都是既有游离态也有化合态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 自然界中大量存在硅单质 | |
| B. | 石英、水晶、硅石的主要成分都是SiO2 | |
| C. | 自然界中SiO2都存在于石英矿中 | |
| D. | SiO2为集成电路和光电池的材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 一定条件下,1 mol A能与3 mol NaOH反应 | |
| B. | 一定条件下,1 mol A能和5 mol氢气发生加成反应 | |
| C. | 一定条件下和浓溴水反应时,1 mol A能消耗3 mol Br2 | |
| D. | A能与碳酸氢钠溶液反应并有气体生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
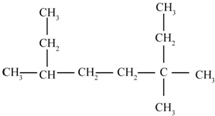 的名称为3,3,6-三甲基辛烷
的名称为3,3,6-三甲基辛烷  的名称为3,6-二甲基-1-庚炔
的名称为3,6-二甲基-1-庚炔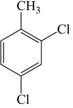 .
. ,其分子式为C15H22O2.
,其分子式为C15H22O2.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com