
| A. | 物质的量是国际单位制中七个基本物理量之一 | |
| B. | 物质的量表示含有一定数目粒子的集体 | |
| C. | 物质的量是国际单位制中的一个基本单位 | |
| D. | 摩尔是计量原子、分子或离子等微观粒子的“物质的量”的单位 |
分析 A.物质的量是1个基本物理量;
B.物质的量描述的是含有一定数目粒子的集体;
C.物质的量是基本物理量,其单位为摩尔;
D.摩尔是物质的量的单位.
解答 解:A.物质的量是1个物理量,是国际单位制中七个基本物理量之一,故A正确;
B.物质的量描述对象为微观离子,表示含有一定数目粒子的集体,故B正确;
C.物质的量是国际单位制中七个基本物理量之一,不是单位,故C错误;
D.摩尔是物质的量的单位,描述对象是原子、分子或离子等微观粒子,故D正确;
故选C.
点评 本题考查了物质的量的应用,题目难度不大,明确物质的量与摩尔之间的关系为解答关键,注意掌握物质的量的描述对象,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加Fe的物质的量 | |
| B. | 将容器的体积缩小一半 | |
| C. | 升高温度 | |
| D. | 压强不变,充入Ne使容器的体积增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向某溶液中滴加KSCN溶液,变为血红色,则原溶液中含有Fe3+ | |
| B. | 向某溶液中滴加NaOH溶液,生成白色沉淀,继而变为灰绿色,最终变为红褐色,则原溶液中含有Fe2+ | |
| C. | 将淀粉和氯化钠的混合溶液装入半透膜中,将半透膜浸泡在盛有蒸馏水的烧杯中,为检验半透膜是否破损,可向蒸馏水中加入硝酸银溶液来验证 | |
| D. | 硫酸亚铁溶液中,常放入一些铁粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
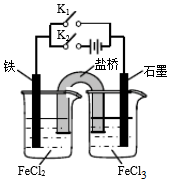
| A. | 闭合K1断开K2,左侧烧杯中的FeCl2溶液浓度逐渐增大 | |
| B. | 闭合K2断开K1,左侧烧杯中的Fe2+向铁电极移动 | |
| C. | 闭合K1断开K2,电流从石墨电极经过K1流向铁电极 | |
| D. | 无论闭合K1断开K2,还是断开K1闭合K2,石墨电极上发生的反应都是Fe3++e-=Fe2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com