
 2NH3
2NH3| 0.8+2.4+0.4 |
| 1+3 |
| ||
| 2min |


 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
| A、①②⑥ | B、①④⑥ |
| C、①③⑥ | D、①②③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 浓H2SO4 |
| 170℃ |

查看答案和解析>>
科目:高中化学 来源: 题型:
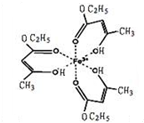 氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示.
氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
4 2 |
56 28 |
132 50 |
208 82 |
16 8 |
17 8 |
18 8 |
16 8 |
17 8 |
18 8 |
298 114 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com