
 DBrCH2CH2Br
DBrCH2CH2Br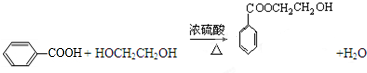 .
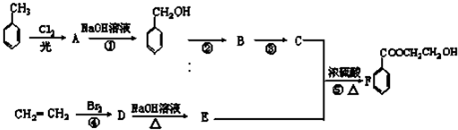
. 分析 甲苯在光照条件下发生甲基上的取代反应生成A,A发生水解反应生成苯甲醇,则A为 ,乙烯与溴发生加成反应生成D为BrCH2CH2Br,D发生水解反应生成E为HOCH2CH2OH,E与C发生酯化反应生成苯甲酸二乙酯,故C为
,乙烯与溴发生加成反应生成D为BrCH2CH2Br,D发生水解反应生成E为HOCH2CH2OH,E与C发生酯化反应生成苯甲酸二乙酯,故C为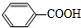 ,则苯甲醇发生氧化反应生成B为
,则苯甲醇发生氧化反应生成B为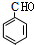 ,苯甲醛发生氧化反应生成苯甲酸,据此解答;
,苯甲醛发生氧化反应生成苯甲酸,据此解答;
解答 解:甲苯在光照条件下发生甲基上的取代反应生成A,A发生水解反应生成苯甲醇,则A为 ,乙烯与溴发生加成反应生成D为BrCH2CH2Br,D发生水解反应生成E为HOCH2CH2OH,E与C发生酯化反应生成苯甲酸二乙酯,故C为
,乙烯与溴发生加成反应生成D为BrCH2CH2Br,D发生水解反应生成E为HOCH2CH2OH,E与C发生酯化反应生成苯甲酸二乙酯,故C为 ,则苯甲醇发生氧化反应生成B为
,则苯甲醇发生氧化反应生成B为 ,苯甲醛发生氧化反应生成苯甲酸,
,苯甲醛发生氧化反应生成苯甲酸,
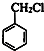
(1)由上述分析可知,A为 ,D为BrCH2CH2Br,
,D为BrCH2CH2Br,
故答案为: ;BrCH2CH2Br;
;BrCH2CH2Br;
(2)反应①是卤代烃发生取代反应,反应④乙烯与溴发生加成反应,故答案为:取代反应;加成反应;
(3)反应⑤的化学方程式为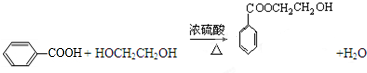 ,
,
故答案为: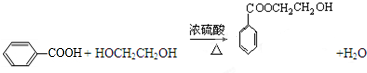 .
.
点评 本题考查有机物推断,注意根据转化关系中有机物的结构进行推断,需要学生熟练掌握官能团的性质与转化,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Cl>P | B. | 氢化物的稳定性:CH4<SiH4 | ||
| C. | 金属性强弱:Na>Li | D. | 酸性:H2CO3>H3PO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
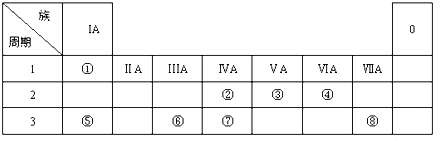
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可选用酚酞作指示剂,溶液由红色变为无色 | |
| B. | 可选用酚酞作指示剂,溶液由无色变为红色 | |
| C. | 可选用甲基橙作指示剂,溶液由黄色变为橙色 | |
| D. | 可选用甲基橙作指示剂,溶液由橙色变为红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不同种元素的原子 | B. | 不同种分子 | ||
| C. | 一种是分子,另一种是离子 | D. | 一种是分子,另一种是原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 药品橱 | 甲 | 乙 | 丙 | 丁 |
| 药品 | 锌、铜 | 硫酸钠 | 氢氧化钠 | 盐酸 |
| 铁、镁 | 碳酸钠 | 氢氧化钾 | 稀硫酸 |
| A. | 甲橱 | B. | 乙橱 | C. | 丙橱 | D. | 丁橱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器中气体密度保持不变 | |
| B. | 容器中混合气体的平均相对分子质量保持不变 | |
| C. | 容器中气体的压强保持不变 | |
| D. | 单位时间内,消耗amol O2的同时生成2amol SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 先加入BaCl2溶液,再加入足量的HNO3溶液,产生了白色沉淀.溶液中一定含有SO42- | |
| B. | 加入足量的HCl溶液,有气体产生,将气体通入澄清石灰水有白色沉淀.溶液中一定含有CO32- | |
| C. | 加入足量浓 NaOH溶液,产生了带有强烈刺激性气味的气体且该气体可以使湿润的红色石蕊试纸变蓝.溶液中一定含有NH4+ | |
| D. | 先加适量的盐酸将溶液酸化,再加AgNO3溶液,产生白色沉淀.溶液中一定含有Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com