
分析 (1)在水溶液或熔融状态下能够导电的化合物为电解质,在水溶液和熔融状态下都不导电的化合物为非电解质,不是化合物的物质既不是电解质,也不是非电解质,据此进行解答;
(2)一水合氨是弱电解质,在水溶液中存在电离平衡,加水稀释时,氢氧根离子物质的量增大;
(3)醋酸是一元弱酸,盐酸是一元强酸,硫酸是二元强酸,pH相同时,氢离子浓度相同,醋酸不完全电离,醋酸浓度远远大于盐酸和硫酸;
(4)醋酸的电离方程式为:CH3COOH?H++CH3COO-,其平衡常数表达式为K=$\frac{c({H}^{+})c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$;据c(H+)=$\sqrt{K×c(C{H}_{3}COOH)}$求算氢离子浓度;
解答 解:(1)电解质为:在水溶液或熔融状态下能够导电的化合物,满足该条件的有①NaCl;②NaOH;③NH3•H2O;⑤BaSO4;⑥H2O;⑦HCl;⑧H2SO4,其中为弱电解质的为③NH3•H2O,⑥H2O,
非电解质为:在水溶液和熔融状态下都不导电的化合物,满足该条件下有:⑨CO2;溶液是混合物,即不是电解质也不是非电解质,
故答案为:③⑥;⑨;
(2)一水合氨是弱电解质,在水溶液中存在电离平衡,加水稀释时,氢氧根离子物质的量增大,NaOH是强电解质,加水稀释时氢氧根离子物质的量不变,加水稀释相同倍数后,一水合氨溶液中氢氧根离子物质的量浓度大,pH大,
故答案为:③;
(3)醋酸是一元弱酸,盐酸是一元强酸,硫酸是二元强酸,pH相同时,醋酸浓度大于盐酸,盐酸浓度大于硫酸;
pH相同时,氢离子浓度相同,醋酸不完全电离,醋酸浓度远远大于盐酸和硫酸,若分别用pH相等的这三种酸中和含等物质的量NaOH的溶液,所需酸溶液的体积醋酸<盐酸=硫酸,
故答案为:④>⑦>⑧;b=c>a;
(4)醋酸的电离方程式为:CH3COOH?H++CH3COO-,其平衡常数表达式为K=$\frac{c({H}^{+})c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$;
c(H+)=$\sqrt{K×c(C{H}_{3}COOH)}$mol/L=$\sqrt{1×1{0}^{-8}×1}$mol/L=1.0×10-4mol/L;
故答案为;1.0×10-4mol/L;
点评 本题考查电解质非电解质的判断、强弱碱加水稀释时pH变化、pH相同的强弱电解质的区别、电离平衡常数的有关计算、pH计算,注意平衡常数只与温度有关,与溶液是酸碱性无关,为易错点.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 将铝片打磨后置于NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ | |
| B. | 向氯化铝溶液中通入过量氨气:4NH3+Al3++2H2O═AlO2-+4NH4+ | |
| C. | 向明矾溶液中加入过量的Ba(OH)2:Al3++2SO42ˉ+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O | |
| D. | 向偏铝酸钠溶液中通入足量CO2:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某试样焰色反应呈黄色,则该试样一定是钠的化合物 | |
| B. | 在石油蒸馏装置中,将温度计水银球插入液面以下 | |
| C. | 在鸡蛋白溶液中加入浓的Na2SO4溶液,可使蛋白质变性 | |
| D. | 用结晶的方法分离氯化钠和硝酸钾的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
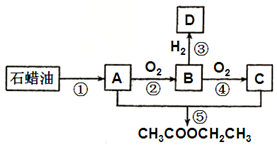 烃A是一种重要的化工原料.已知A在标准状况下的密度为1.25g•L-1,B可发生银镜反应.它们之间的转化关系如图:
烃A是一种重要的化工原料.已知A在标准状况下的密度为1.25g•L-1,B可发生银镜反应.它们之间的转化关系如图:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用量筒量取所需浓盐酸倒入烧杯后,用水洗量筒2~3次,洗液倒入烧杯中 | |
| B. | 定容时仰视刻度线 | |
| C. | 用量筒量取所需的浓盐酸时俯视刻度 | |
| D. | 定容后倒转容量瓶几次,发现凹液面最低点低于刻度线,补几滴水达到刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 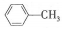 的一溴代物和 的一溴代物和 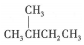 的一溴代物都有4种(不考虑立体异构) 的一溴代物都有4种(不考虑立体异构) | |
| B. | CH3CH=CHCH3分子中的四个碳原子在同一直线上 | |
| C. | 按系统命名法,化合物 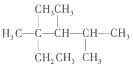 的名称是2,3,4-三甲基-2-乙基戊烷 的名称是2,3,4-三甲基-2-乙基戊烷 | |
| D. | 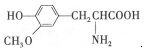 与 与 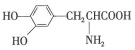 都是α-氨基酸且互为同系物 都是α-氨基酸且互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
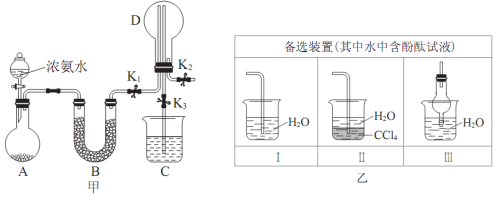
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com