
取少量Fe2O3粉末(红棕色)加入适量盐酸,发生反应的化学方程式: ,
反应后得到的溶液呈 色。用此溶液分别做如下实验:
(1)取少量溶液置于试管中,滴入几滴NaOH溶液,可观察到有红褐色沉淀生成,反应的化学方程式为 ,此反应属于 (填反应类型)。
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈 色,即制得Fe(OH)3胶体。
(3)取另一只小烧杯也加入20 mL蒸馏水,向烧杯中加入1 mL FeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到 烧杯中的液体产生丁达尔效应。这个实验可以用来区别 。
(4)用Fe(OH)3胶体进行下列实验:
①将其装入U形管中,用石墨电极接通直流电,通电一段时间后,发现阴极附近的颜色加深,这说明 ,这种现象称为 。
②向其中加入饱和(NH4)2SO4溶液发生的现象是 ,原因是 ,
③向其中滴入过量稀硫酸,现象是 ,其原因是 。
④提纯此分散系常用的方法是 。
Fe2O3+6HCl=2FeCl3+3H2O (棕)黄
(1)FeCl3+3NaOH=3NaCl+Fe(OH)3↓ 复分解反应 (2)红褐 (3)乙 胶体和溶液
(4)①Fe(OH)3胶体粒子带正电荷 电泳 ②产生红褐色沉淀 电解质溶液使胶体发生了聚沉 ③先出现红褐色沉淀,后沉淀溶解 开始加入稀硫酸时,胶体发生聚沉生成氢氧化铁沉淀,当酸过量时又使沉淀溶解 ④渗析法
【解析】碱性氧化物与酸反应生成盐和水,即Fe2O3+6HCl=2FeCl3+3H2O,FeCl3溶液呈棕黄色。
(1)向FeCl3溶液中滴入NaOH溶液发生复分解反应。(2)此小题主要考查Fe(OH)3胶体的制法。(3)胶体可产生丁达尔效应,而溶液不能,利用这一点可以区分胶体和溶液。(4)①阴极附近颜色加深,说明阴极附近Fe(OH)3胶体胶粒浓度变大,胶粒向阴极发生了移动,说明Fe(OH)3胶体粒子带负电荷;②加入电解质(NH4)2SO4饱和溶液后,胶体发生聚沉生成了红褐色沉淀;③加入稀硫酸,开始电解质使胶体聚沉生成沉淀,然后发生反应2Fe(OH)3+3H2SO4=Fe2(SO4)3+6H2O,使沉淀溶解;④胶粒不能通过半透膜,而小分子、离子等可以通过半透膜,因此可用渗析法提纯胶体。


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源:2014年高考化学苏教版总复习 1-1 物质的分类、转化及分散系练习卷(解析版) 题型:填空题
“探险队员”——盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质或水溶液),盐酸必须避开它们,否则就无法通过。
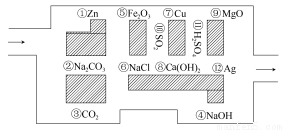
(1)请你帮助它走出迷宫 (请用图中物质前的序号连接起来表示所走的路线)。
(2)在能“吃掉”盐酸的化学反应中,属于酸碱中和反应的有 个,属于氧化还原反应的有 个,其中能“吃掉”盐酸的盐是 ,写出该反应的离子方程式: 。
(3)在不能与盐酸反应的物质中,属于电解质的是 ,属于非电解质的是 (填写物质序号)。
(4)如果将盐酸换成氯气,它能沿着盐酸走出的路线“走出”这个迷宫吗?为什么? 。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习3-1钠、镁及其化合物练习卷(解析版) 题型:选择题
下列关于Na2CO3和NaHCO3性质的说法错误的是 ( )。
A.热稳定性:NaHCO3<Na2CO3
B.与同浓度盐酸反应的剧烈程度:NaHCO3<Na2CO3
C.相同温度时,在水中的溶解性:NaHCO3<Na2CO3
D.等物质的量浓度溶液的pH:NaHCO3<Na2CO3
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习2-3-1氧化还原反应概念和规律练习卷(解析版) 题型:选择题
氧化还原反应与四种基本反应类型的关系如图所示,则下列化学反应属于阴影部分的是 ( )。
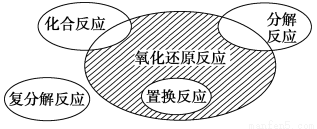
A.Cl2+2KBr=Br2+2KCl
B.2NaHCO3 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
C.4Fe(OH)2+O2+2H2O=4Fe(OH)3
D.2Na2O2+2CO2=2Na2CO3+O2
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习2-2电解质 离子反应练习卷(解析版) 题型:选择题
下列离子或分子组能大量共存,且满足相应要求的是( )。
选项离子或分子要求
AK+、NO3-、Cl-、HCO3-c(K+)<c(Cl-)
BCa2+、NO3-、SO32-、Cl-滴加盐酸立即有气体产生
CNH4+、Al3+、SO42-、Br-逐滴滴加NaOH溶液立即有气体产生
DNa+、HCO3-、Mg2+、SO42-滴加氢氧化钠溶液立即有沉淀产生
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习2-1物质的分类与转化 分散系练习卷(解析版) 题型:选择题
若将NaOH(s)、P2O5(s)、无水CaCl2(s)归为一类。从A~D中选出一种最适宜与这三种物质归为一类的物质是 ( )。
A.浓硫酸 B.氯化氢 C.纯碱 D.生石灰
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习1-2-2溶液的配制及误差分析练习卷(解析版) 题型:填空题
(Ⅰ)下列操作会导致实验结果偏高的是 。
A.配制一定物质的量浓度的硫酸溶液时,定容摇匀后,发现液面低于刻度线
B.在配制一定物质的量浓度溶液时,用10 mL的量筒量取5.0 mL液体溶质时俯视读数
C.用天平称量20.5 g某物质,砝码和药品的位置放反,所得药品的质量
D.配制一定物质的量浓度的溶液时,定容时俯视读数,所得溶液的浓度
(Ⅱ)现有下列仪器或用品:
a铁架台(含铁圈、铁夹);b锥形瓶;c滴定管;d烧杯(若干);e玻璃棒;f胶头滴管;g托盘天平(含砝码);h滤纸;i量筒;j漏斗;k温度计
现有下列试剂:
A.NaOH固体 B.碳酸钠溶液
C.氯化镁溶液 D.蒸馏水
试填空:
(1)如图分别是温度计、量筒、滴定管的一部分,下述判断及读数(虚线刻度)不正确的是 。
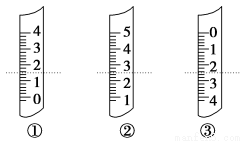
A.①是量筒,读数为1.5 mL
B.②是量筒,读数为2.50 mL
C.③是滴定管,读数为2.50 mL
D.①是温度计,读数是1.50 ℃
(2)配制100 mL 0.1 mol·L-1的氢氧化钠溶液时,还缺少的仪器有 。
(3)除去Mg(OH)2中混有的少量Ca(OH)2,可以用到的试剂是 (选填序号),操作方法是 、 、洗涤。
完成上述操作,上述仪器或用品用到的有 (从上述仪器或用品中选择,填上相应序号)。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习1-2-1物质的量 气体摩尔体积练习卷(解析版) 题型:选择题
下列每组分别给出了两个量,其中可以求出物质的量的有( )。
① | ② | ③ | ④ | ⑤ |
物质所含的微粒数 | 固体体积 | 溶液的质量分数 | 标准状况下气体的摩尔体积 | 非标准状况下某物质的质量 |
阿伏加德罗常数 | 固体密度 | 溶液体积 | 标准状况下气体的体积 | 物质的摩尔质量 |
A.①②⑤ B.②③④ C.①④⑤ D.①③④
查看答案和解析>>
科目:高中化学 来源:2014年高考化学考前题型专练 保温训练(三)(解析版) 题型:选择题
下列图示与对应的叙述相符的是 ( )。
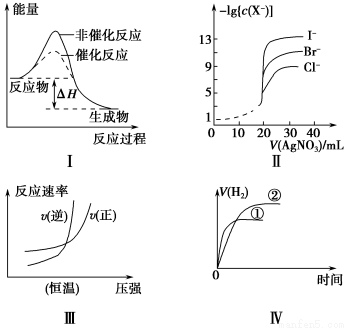
A.图Ⅰ中ΔH表示某一反应有无催化剂的反应热相同
B.用0.010 0 mol·L-1硝酸银标准溶液,滴定浓度均为0.100 0 mol·L-1 Cl-、Br-及I-的混合溶液,由图Ⅱ曲线,可确定首先沉淀的是Cl-
C.图Ⅲ可表示工业合成氨反应在温度一定的情况下反应速率与压强的关系
D.图Ⅳ表示相同体积、相同pH的一元强酸溶液①和一元弱酸溶液②分别与足量的锌粉发生反应,V(H2)随时间的变化曲线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com