
【题目】解释下列事实的方程式正确的是
A.用碳酸钠溶液处理水垢中的硫酸钙:Ca2++CO32-=CaCO3↓
B.SO2使紫色石蕊溶液变红色:SO2+H2O=2H++SO32-
C.用石墨电极电解AlCl3溶液,阴极附近生成沉淀:2Al3++6H2O+6e- =2Al(OH)3↓+3H2↑
D.工业上制取硅:SiO2+C![]() Si+CO2
Si+CO2
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】25℃、101 kPa下,2g氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是( )
A. 2H2(g)+O2(g) == 2H2O(1) △H= ―285.8kJ/mol![]()
B. 2H2(g)+ O2(g) == 2H2O(1) △H= +571.6 kJ/mol
C. 2H2(g)+O2(g) == 2H2O(g) △H= ―571.6 kJ/mol
D. H2(g)+1/2O2(g) == H2O(1) △H= ―285.8kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应A(g)+3B(g)![]() 2C(g)+2D(g) 在4种不同情况下反应速率分别如下,其中反应速率v最大的是
2C(g)+2D(g) 在4种不同情况下反应速率分别如下,其中反应速率v最大的是
A. v(A)=0.15mol/(L·min) B. v (B)=0.6 mol/(L·min)
C. v (C)=0.3 mol/(L·min) D. v (D)=0.1 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:
实验一 焦亚硫酸钠的制取
采用如图装置(实验前已除尽装置内的空气)制取Na2S2O5。装置Ⅱ中有Na2S2O5晶体析出,发生的反应为:Na2SO3+SO2=Na2S2O5
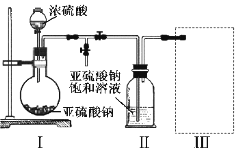
(1)装置I中产生气体的化学方程式为__________________。
(2)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是_________。
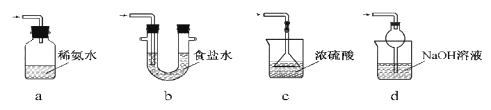
(3)装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为________(填序号)。
实验二 焦亚硫酸钠的性质
Na2S2O5溶于水即生成NaHSO3。
(4)证明NaHSO3溶液中HSO3-的电离程度大于水解程度,可采用的实验方法是________(填序号)。
a.测定溶液的pH b.加入Ba(OH)2溶液 c.加入盐酸
d.加入品红溶液 e.用蓝色石蕊试纸检测
(5)检验Na2S2O5晶体在空气中已被氧化的实验方案是____________。
实验三 葡萄酒中抗氧化剂残留量的测定
(6)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

(已知:滴定时反应的化学方程式为SO2+I2+2H2O=H2SO4+2HI)
①按上述方案实验,消耗标准I2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为________________g·L-1。
②在上述实验过程中,若有部分HI被空气氧化,则测得结果____(填“偏高”“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸镍[(CH3COO)2Ni]是一种重要的化工原料,一种以含镍废料(含 NiS、Al2O3、FeO、CaO、SiO2)为原料,制取醋酸镍的工艺流程图如下:
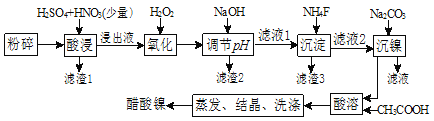
相关离子生成氢氧化物的pH和相关物质的溶解性如表:
金属离子 | 开始沉淀的pH | 沉淀完全的pH | 物质 | 20℃时溶解性(H2O) | |
Fe3+ | 1.1 | 3.2 | CaSO4 | 微溶 | |
Fe2+ | 5.8 | 8.8 | NiF | 可溶 | |
Al3+ | 3.0 | 5.0 | CaF2 | 难溶 | |
Ni2+ | 6.7 | 9.5 | NiCO3 | Ksp=9.6×10﹣6 |
(1)调节pH步骤中,溶液pH的调节范围是___________。
(2)滤渣1主要成分是_______________;滤渣2主要成分是_________________
(3)写出氧化步骤中加入H2O2发生反应的离子方程式_________。
(4)酸浸过程中,1mol NiS失去6NA个电子,同时生成两种无色有毒气体。写出该反应的化学方程式____________。
(5)沉镍过程中,若c(Ni2+)=2.0mol/L,欲使100mL该滤液中的Ni2+沉淀物完全,[c(Ni2+)≤10﹣5 mol/L],则需要加入Na2CO3固体的质量最少为_____g(保留小数点后1位)
(6)保持其他条件不变,在不同温度下对含镍废料进行酸浸。酸浸出率随时间变化如图。酸浸的最佳温度与时间分别为____________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是实验室制备气体的有关内容:
编号 | 实验内容 | 实验原理 |
① | 制氧气 | H2O2→O2 |
② | 制氨气 | NH4Cl→NH3 |
③ | 制氯气 | HCl→Cl2 |
(1)上述气体中:从制备过程看,必须选择合适的氧化剂才能实现的是_________(填气体的化学式,下同);从反应中有无电子转移的角度看,明显不同于其他气体的是______,写出实验室制取该气体的化学方程式_______________________________
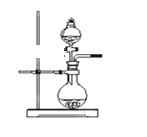
(2)若用上述装置制备NH3,则选择的试剂为____________________。
(3)制备Cl2需用8 mol/L的盐酸100mL,现用12 mol/L的盐酸来配制。
①需要12 mol/L的盐酸的体积为__________mL(精确到0.1 mL)
②在容量瓶的使用方法中,下列操作不正确的是_______________(填写标号)。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时用量筒量取浓盐酸后用玻璃棒引流入容量瓶中,缓慢加入蒸馏水到接近标线1cm~2cm处,用胶头滴管滴加蒸馏水直到凹液面的最低处和标线相平
D.定容后盖好瓶塞,用食指顶住,用另一只手手指托住瓶底,把容量瓶倒转和摇动多次
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数依次增大的五种短周期主族元素X、Y、Z、P、Q分别位于三个周期,X与Z、Y与P分别位于同主族,Z与Y可形成原子个数比分别为1∶1和2∶1的离子化合物。则下列说法正确的是![]()
A. 简单氢化物的沸点:Q>Y
B. 简单氢化物的热稳定性:Y>Q>P
C. 非金属性强弱:Q>P>Y>X
D. X、Y、Z、P形成的化合物的水溶液显碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物W用作调香剂、高分子材料合成的中间体等,制备W的一种合成路线如下。

已知:![]() +CH3Cl
+CH3Cl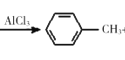 +HCl
+HCl
请回答下列问题
(1)F的化学名称是__________,②的反应类型是__________。
(2)D中含有的官能团是__________(写名称),D聚合生成高分子化合物的结构简式为__________。
(3)反应③的化学方程式是____________________________________________。
(4)反应⑥的化学方程式是_______________________________________________。
(5)芳香化合物N是A的同分异构体,其中核磁共振氢谱为三组峰的结构简式为__________。
(6)参照有机物W的上述合成路线,设计以M为起始原料制备F的合成路线(无机试剂任选)。![]() __
__
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。
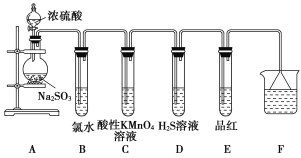
请回答下列问题:
(1)装置A中盛放浓硫酸的仪器名称是___________。
(2)反应后,装置B中发生的现象是反应的离子方程式为____________;装置C中的现象是___________,表现了SO2的________ 性;装置D中现象是____________,发生反应的化学方程式为_____________________。
(3)装置E的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象____。
(4)F装置的作用是________________漏斗的作用是________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com