
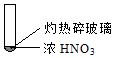 | 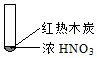 | 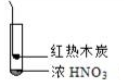 |
| ① | ② | ③ |
| A. | 由①中的红棕色气体,推断产生的气体一定是混合气体 | |
| B. | 红棕色气体不能表明②中木炭与浓硝酸产生了反应 | |
| C. | 由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物 | |
| D. | ③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应 |
分析 题中涉及实验都在加热条件下,浓硝酸不稳定,加热分解生成的二氧化氮气体为红棕色,且加热条件下,浓硝酸可与碳发生氧化还原反应,以此解答该题.
解答 解:A.加热条件下,浓硝酸分解生成二氧化氮和氧气,则产生的气体一定是混合气体,故A正确;
B.在加热条件下,浓硝酸可分解生成二氧化氮,不一定与碳反应生成,故B正确;
C.硝酸中N元素化合价为+5价,生成二氧化氮的N元素化合价为+4价,化合价降低,在生成的红棕色气体为还原产物,故C正确;
D.碳加热至红热,可与空气中氧气反应生成二氧化碳,不一定是与浓硝酸发生了反应,故D错误.
故选D.
点评 本题为2017年北京考题,考查浓硝酸的性质,侧重考查学生的分析能力和元素化合物知识的综合理解和运用,注意把握物质的性质以及实验的严密性和可行性的评价,难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | PH3分子呈三角锥形 | |
| B. | PH3分子是极性分子 | |
| C. | PH3中P 采取sp2杂化 | |
| D. | PH3分子稳定性低于NH3分子,因为N-H键键能高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 目的 | 操作 | |
| A. | 取20.00 mL盐酸 | 在50 mL酸式滴定管中装入盐酸,调整初始读数为30.00mL后,将剩余盐酸放入锥形瓶 |
| B. | 清洗碘升华实验所用试管 | 先用酒精清洗,再用水清洗 |
| C. | 测定醋酸钠溶液pH | 用玻璃棒蘸取溶液,点在湿润的pH试纸上 |
| D. | 配制浓度为0.010 mol•L的KMnO4溶液 | 称取KMnO4固体0.158 g,放入100 mL容量瓶中,加水溶解并稀释至刻度 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ”,tián),Ts的原子核外最外层电子数是7,下列说法不正确的是( )
”,tián),Ts的原子核外最外层电子数是7,下列说法不正确的是( )| A. | Ts是第七周期第ⅦA族元素 | |
| B. | Ts的同位素原子具有相同的电子数 | |
| C. | Ts在同族元素中非金属性最弱 | |
| D. | 中子数为176的Ts核素符号是${\;}_{117}^{176}$Ts |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极a常用掺有石墨烯的S8材料,电池反应为:16Li+xS8=8Li2Sx(2≤x≤8).下列说法错误的是( )
全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极a常用掺有石墨烯的S8材料,电池反应为:16Li+xS8=8Li2Sx(2≤x≤8).下列说法错误的是( )| A. | 电池工作时,正极可发生反应:2Li2S6+2Li++2e-=3Li2S4 | |
| B. | 电池工作时,外电路中流过0.02 mol电子,负极材料减重0.14 g | |
| C. | 石墨烯的作用主要是提高电极a的导电性 | |
| D. | 电池充电时间越长,电池中的Li2S2量越多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用石灰、碳酸钠等碱性物质处理废水中的酸 | |
| B. | 用可溶性的铝盐和铁盐处理水中的悬浮物 | |
| C. | 用氯气处理水中的Cu2+、Hg2+等重金属离子 | |
| D. | 用烧碱处理含高浓度NH4+的废水并回收利用氨 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 活性炭具有还原性,可用作冰箱除味剂 | |
| B. | 二氧化硫具有氧化性,可用作造纸漂白剂 | |
| C. | Al2O3具有很高的熔点,可用于制造熔融烧碱的坩埚 | |
| D. | FeCl3溶液能与Cu反应,可用于蚀刻印刷电路板 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com