

分析 (1)根据配制一定物质的量浓度溶液用到仪器选择;根据配制溶液的体积选择容量瓶的规格;
(2)依据容量瓶构造及正确使用方法解答;
(3)依据m=CVM计算需要溶质的质量;定容时仰视刻度线,导致溶液体积偏大,依据C=$\frac{n}{V}$进行误差分析;
(4)据c=$\frac{1000ρω}{M}$计算浓硫酸的物质的量浓度,依据溶液稀释前后溶质的物质的量不变计算需要浓硫酸的体积,依此选择合适的量筒.
解答 解:(1)要配置450ml溶液应选择500ml容量瓶,配制一定物质的量浓度溶液用的仪器有:托盘天平、药匙、烧杯、筒量、玻璃棒、容量瓶、胶头滴管,不需要的仪器有烧瓶和分液漏斗,还缺少的仪器:烧杯、玻璃棒、500mL容量瓶,
故答案为:AC;烧杯、玻璃棒、500mL容量瓶;
(2)A.在容量瓶的使用方法中,A.使用容量瓶前应该检验是否漏水,故A正确;
B.容量瓶用水洗净后,不能用待配溶液洗涤,否则会影响配制溶液的浓度,故B错误;
C.容量瓶为精密仪器,不能在容量瓶中溶解固体,故C错误;
D.容量瓶为精密仪器,不能在容量瓶中稀释浓溶液,故C错误;
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀,故E正确;
故选:BCD;
(3)需要0.1mol/LNaOH溶液450mL,实验室没有450mL容量瓶,应选择500mL容量瓶,实际配制500mL溶液,需要溶质的质量m=0.1mol/L×40g/mol×0.5L=2.0g;
定容时仰视刻度线,导致溶液体积偏大,依据C=$\frac{n}{V}$可知,溶液浓度偏低,小于0.1mol/L;
故答案为:2.0;小于;
(4)质量分数为98%、密度为1.84g/cm3的浓硫酸的物质的量浓度=$\frac{1000×1.84×98%}{98}$=18.4mol/L,浓硫酸稀释前后溶质的物质的量不变,设浓硫酸的体积为V,所以18.4mol/L×V=0.5/L×0.5L,V=0.0136L=13.6mL,应选择15ml量筒;
故答案为:13.6;15.
点评 本题考查一定物质的量浓度溶液的稀释,熟悉配制原理、注意容量瓶、量筒规格的选取方法,题目难度不大.


科目:高中化学 来源: 题型:选择题
| 选项 | 化学反应方程式 | 已知条件 | 预测 |
| A | M(s)═X(g)+Y(s) | △H>0 | 它是非自发反应 |
| B | W(s)+xG(g)═20Q(g) | △H<0,自发反应 | x可能等于1、2、3 |
| C | 4X(g)+5Y(g)═4W(g)+6G(g) | 能自发反应 | △H一定小于0 |
| D | 4M(s)+N(g)+2W(l)═4Q(s) | 常温下,自发进行 | △H>0 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知某温度下:
已知某温度下: (g)?
(g)? (g)+H2(g),△H=+117.6kJ/mol.
(g)+H2(g),△H=+117.6kJ/mol. (g)?
(g)? (g)+CO(g)+H2O(g)△H=+158.8 kJ/mol.该反应的化学平衡常数K=K1•K2(用K1、K2表示).
(g)+CO(g)+H2O(g)△H=+158.8 kJ/mol.该反应的化学平衡常数K=K1•K2(用K1、K2表示).| T/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
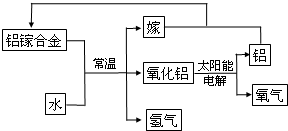 铝是地壳中含量最多的金属元素,其单质和化合物广泛应用于日常生活中.
铝是地壳中含量最多的金属元素,其单质和化合物广泛应用于日常生活中.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | K+ Cu2+ Fe3+ Al3+ Fe2+ |
| 阴离子 | Cl- CO${\;}_{3}^{2-}$ NO${\;}_{3}^{-}$ SO${\;}_{4}^{2-}$ SiO${\;}_{3}^{2-}$ |
| 选项 | 污染物 | 处理措施 | 方法类别 |
| A | 废酸 | 加生石灰中和 | 物理法 |
| B | Cu2+等重金属离子 | 加硫酸盐沉降 | 化学法 |
| C | 含复杂有机物的废水 | 通过微生物代谢 | 物理法 |
| D | 碱性的废水 | 用CO2中和 | 化学法 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 0min | 5min | 10min | |
| CO | 0.01 | 0.0056 | |
| H2O | 0.01 | 0.0156 | |
| CO2 | 0 | 0.0044 | |
| H2 | 0 | 0.0044 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 现代生活离不开铝,铝有许多优良的性能,因此在各方面有极其广泛的用途.
现代生活离不开铝,铝有许多优良的性能,因此在各方面有极其广泛的用途.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H3=△H1+2△H2 | B. | △H3=△H1+△H2 | C. | △H3=△H1-2△H2 | D. | △H3=△H1-△H2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com