
| A. | 1L 1 mol/L CH3COONa溶液中存在NA个CH3COO- | |
| B. | 标况下,22.4L 甲醇中所含原子数一定为6NA | |
| C. | 1mol CnH2n+2含有(3 n+1)NA个共价键 | |
| D. | 0.1mol羟基含有的电子数为NA |
分析 A、醋酸是弱酸存在电离平衡;
B、甲醇在标准状况下不是气体;
C、烷烃中碳碳间共用电子对数为碳原子数减去1;碳氢电子对数与H原子个数相同,据此计算即可;
D、羟基的化学式为-OH,不显电性.
解答 解:A、醋酸是弱酸存在电离平衡,1L 1 mol/L CH3COONa溶液中存在CH3COO-小于NA个,故A错误;
B、标况下,甲醇不是气体,22.4L 甲醇物质的量不是1mol,故B错误;
C、分子式为CnH2n+2的烃分子中,碳原子数为n,则烷烃中碳碳间共用电子对数为n-1,C-H的对数为2n+2,故1molCnH2n+2的总电子对数为:n-1+2n+2=3n+1,含有(3 n+1)NA个共价键,故C正确;
D、羟基的化学式为-OH,不显电性,故0.1mol羟基含0.9mol电子,0.9NA,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:解答题

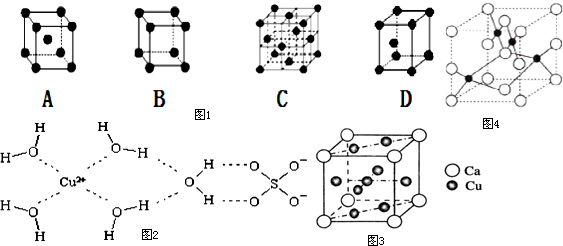
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1000 mL | B. | 500 mL | C. | 100 mL | D. | 1500 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蛋白质和葡萄糖在一定条件下完全燃烧都只生成CO2和水 | |
| B. | 75%(体积分数)的乙醇溶液常用于医疗消毒 | |
| C. | 石油的分馏和煤的干馏均属于物理变化 | |
| D. | 乙烯和苯都能使溴水褪色,褪色的原因相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
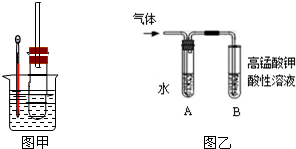 用如图实验装置(铁架台、酒精灯略) 验证溴乙烷的性质:
用如图实验装置(铁架台、酒精灯略) 验证溴乙烷的性质:查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C(Na+)>C(HCO3-)>C(CO32-)>C(H+)>C(OH-) | B. | C(Na+)>C[H+]=C[HCO3-]+C[CO32-]+C[OH-] | ||
| C. | C[Na+]+C[H+]=C[HCO3-]+2C[CO32-]+C[OH-] | D. | C[Na+]=C[HCO3-]+C[CO32-] |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com