
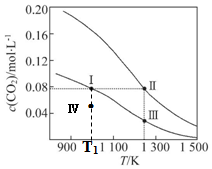
| A. | 该反应的△H>0、△S<0 | B. | 体系的总压强p:p (Ⅰ)>p (Ⅲ) | ||
| C. | 平衡常数:K(Ⅰ)>K (Ⅱ) | D. | T1K时,Ⅳ点所处的状态中 v(正)<v(逆) |
分析 由图象可知升高温度,CO2的浓度减小,说明平衡正向移动,则正反应为吸热反应,对于CO2(g)+C(s)?2CO(g)反应来说,生成物气体的计量数较大,增大压强,平衡逆向移动,CO2的浓度增大,以此解答该题.
解答 解:A.生成物气体的计量数较大,则△S>0,故A错误;
B.正反应为吸热反应,升高温度,气体的物质的量增大,压强增大,故B错误;
C.正反应为吸热反应,升高温度,平衡正向移动,则平衡常数增大,故C错误;
D.Ⅳ点为达到平衡,如达到平衡,则c(CO2)应增大,向逆向移动,则v(正)<v(逆),故D正确.
故选D.
点评 本题考查化学平衡及平衡的建立,为高频考点,侧重考查学生的分析能力,把握平衡移动的影响因素、图象分析为解答的关键,选项D为解答的难点,题目难度中等.


科目:高中化学 来源: 题型:解答题
 )是一种重要的化工原料,下面是以环戊烷为原料制备环戊二烯的合成路线:
)是一种重要的化工原料,下面是以环戊烷为原料制备环戊二烯的合成路线: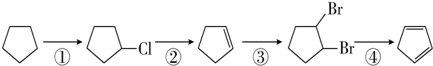
 ),途径如下:
),途径如下: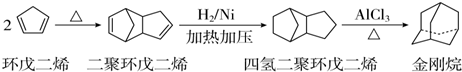
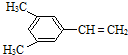 、
、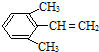 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 200mL 2mol/L MgCl2溶液 | |
| B. | 1000mL 2.5mol/L NaCl溶液 | |
| C. | 10g AgCl固体加入 300mL水充分搅拌 | |
| D. | 250mL 1mol/L AlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3a+b-c | B. | c+3a-b | C. | a+b-c | D. | c+a-b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | p(甲)<p(乙)<p(丙) | B. | p(甲)>p(乙)>p(丙) | C. | p(甲)<p(丙)<p(乙) | D. | p(乙)>p(甲)>p(丙) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=4的0.1mol/L NaHA溶液:c(HA-)>c(H+)>c(A2-)>c(OH-)>c(H2A) | |
| B. | 10mL 0.1mol/L CH3COOH溶液与20mL 0.1mol/L NaOH溶液混合后,溶液中离子浓度关系:c(OH-)=c(H+)+c(CH3COO-)+2c(CH3COOH) | |
| C. | 两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1<10c2 | |
| D. | 已知:HA为弱酸,则两种溶液①0.1mol/LHA溶液;②0.3mol/LHA溶液与0.1mol/LNaOH溶液等体积的混合液,c(H+)①>② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
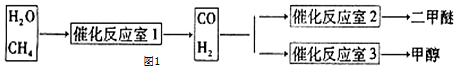

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| B. | 由C(金刚石)→C(石墨)△H=-1.9KJ/mol 可知,金刚石比石墨稳定 | |
| C. | 在101Kpa时,2gH2完全燃烧生成液态水,放出285.8KJ热量,氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l)△H=+285.8KJ/mol | |
| D. | 稀溶液中:H+(aq)+OH-(aq)=H2O(l)△H=-53.7KJ/mol,若将含1 mol CH3COOH与含1 mol NaOH的溶液混合,放出的热量小于53.7KJ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
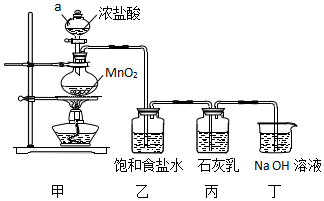
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com