
| A. | ①④⑤⑥ | B. | ①②⑤⑥ | C. | ①③④⑤ | D. | 全部 |
分析 ①依据氧化铝熔点高性质解答;
②明矾溶于水,铝离子水解生成的具有吸附作用的氢氧化铝胶体;
③氧化铁为红棕色固体;
④碳酸氢钠不稳定,受热分解生成二氧化碳;
⑤依据焰色反应解答;
⑥过氧化钠与水、二氧化碳反应生成氧气.
解答 解:①Al2O3熔点高,耐高温,可以作耐火坩埚,故正确;
②明矾溶于水,铝离子水解生成的具有吸附作用的氢氧化铝胶体,可以净水,不具有杀菌消毒作用,故错误;
③氧化铁为红棕色固体;,用于制造红色油漆和涂料,故错误;
④碳酸氢钠不稳定,受热分解生成二氧化碳,常用作食品发酵剂,故正确;
⑤含不同金属元素的物质灼烧产生不同焰色,所以钠、钾、锶、钡等化合物(作烟花的焰色),故正确;
⑥过氧化钠与水、二氧化碳反应生成氧气,所以过氧化钠通常可用作供氧剂,故正确;
故选:A.
点评 本题考查了元素化合物知识,侧重考查物质的用途,熟悉相关物质的性质和用途是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 可将地下输油钢管与外加直流电源的负极相连以保护钢管不受腐蚀 | |
| B. | 常温条件下,铝在空气中不易被腐蚀 | |
| C. | 镀层破坏后,白铁(镀锌的铁)比马口铁(镀锡的铁)更耐腐蚀 | |
| D. | 用锌与稀硫酸刮氢气时,往稀硫酸中滴少量硫酸铜溶液能加快反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只用肉眼就可以把胶体和溶液、浊液区别开来 | |
| B. | 向Fe(OH)3胶体中滴加少量H2SO4溶液,会生成红褐色沉淀 | |
| C. | 用渗析的方法净化胶体时,使用的半透膜只能让较小的分子、离子透过 | |
| D. | 胶粒的表面积较大,微粒具有较大的表面积,能吸附阳离子或阴离子,故在电场作用下会产生电泳现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2S?2H++S2- | B. | H2S+H2O?H3O++HS- | ||
| C. | HCl?H++Cl- | D. | HClO═H++ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
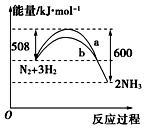 N2与H2反应生成NH3的过程中能量变化曲线如图所示.若在一个容积固定的密闭容器中充入1mol N2和 3mol H2使反应N2+3H2?2NH3达到平衡,测得反应放出热量为Q kJ
N2与H2反应生成NH3的过程中能量变化曲线如图所示.若在一个容积固定的密闭容器中充入1mol N2和 3mol H2使反应N2+3H2?2NH3达到平衡,测得反应放出热量为Q kJ查看答案和解析>>
科目:高中化学 来源: 题型:解答题
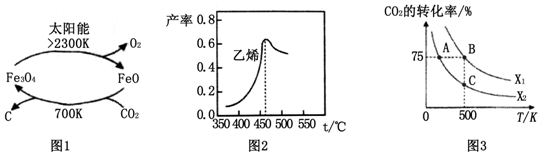
| 时间/min 浓度/mol•L-1 | 0 | 10 | 20 | 30 | 40 | 50 |
| H2(g) | 6.00 | 5.40 | 5.10 | 9.00 | 8.40 | 8.40 |
| CO2(g) | 2.00 | 1.80 | 1.70 | 3.00 | 2.80 | 2.80 |
| CH2=CH2(g) | 0 | 0.10 | 0.15 | 0.50 | 0.60 | 0.60 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com