
| A、将2mol NO和1molO2混合后,体系中的原子总数为6NA |
| B、0.01mol Mg在CO2中完全燃烧,转移电子数为0.01NA |
| C、标准状况下,3.2gCu与足量的浓硝酸反应生成气体的分子数为0.2NA |
| D、7.8Na2O2含有的阴离子数为0.2NA |
| m |
| M |
| 3.2g |
| 64g/mol |
| 7.8g |
| 78g/mol |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、标准标况下,22.4L水所含的分子数目为6.02×1023个 |
| B、2g氢气所含氢原子数目为2×6.02×1023个 |
| C、500ml2mol?L-1的Ba(NO3)2溶液中含NO3-离子数为2×6.02×1023个 |
| D、0.5mol氯气分子中含Cl原子数为6.02×1023个 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Na+、NO3-、MnO4- |
| B、K+、Na十、Br-、CO32- |
| C、Mg2+、Na+、Cl-、SO42- |
| D、Na十、Ba2+、OH-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、滤去不溶性杂质以后,将滤液移至坩埚内加热浓缩 |
B、右图能用作防倒吸装置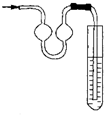 |
| C、蒸馏时,通过冷凝管冷凝得到的液体直接用锥形瓶接收 |
| D、称量NaOH固体时,应将砝码放在托盘天平右盘纸片上,NaOH固体放在左盘的纸片上 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH3?H2O═NH4++OH- |
| B、H2CO3?CO32-+2H+ |
| C、NaHCO3═Na++H++CO32- |
| D、Al2(SO4)3═2Al3++3SO42- |
| E、Al2(SO4)3═2Al3++3SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、大量进口石油,减少煤炭使用量 |
| B、回收废弃饮料包装纸,制作成公园内的休闲长椅 |
| C、在西部和沿海地区兴建风力发电站,解决能源问题 |
| D、鼓励购买小排量汽车,推广与发展电动、混合动力汽车 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有①②④⑤ | B、只有②③⑤ |
| C、只有①②③⑤ | D、全部 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com