
【题目】X、Y、Z、R、M是原子序数依次增大的五种元素,基态X原子的s电子数比p电子数多3个,Y、Z均位于第二周期且两元素最外层电子数之和为11, Z、R同主族,M核外电子有26种运动状态,请回答下列问题:
(1)化合物XCl3中心原子的杂化轨道类型为_______;RC12的立体构型为________。
(2)H2Z、H2R的沸点分别为100℃、-60.4℃,试解释其原因:______________。
(3)R、M形成的一种化合物晶胞如图所示。

① 该化合物的化学式为________;
② 若晶胞参数为a pm。列式计算该晶胞的密度ρ=_______g/cm3。
【答案】 sp2 V形 H2O分子间可以形成氢键,H2S分子间不能形成氢键 FeS2 ![]()
【解析】X、Y、Z、R、M是原子序数依次增大五种元素,M核外电子有26种运动状态,则M为Fe;基态X原子的s电子数比p电子数多3个,原子核外电子排布式为1s22s22p1,则X为B元素;Y、Z均位于第二周期且两元素最外层电子数之和为11, Z、R同主族,故Y为N元素、Z为O元素、R为S元素;
(1)化合物BCl3中B原子孤电子对数=![]() =0,价层电子对数=3+0=3,其B原子杂化方式为sp2;SCl2分子中S原子价层电子对个数是4且含有2个孤电子对,所以该分子空间构型是V形;
=0,价层电子对数=3+0=3,其B原子杂化方式为sp2;SCl2分子中S原子价层电子对个数是4且含有2个孤电子对,所以该分子空间构型是V形;
(2)H2O分子间可以形成氢键,H2S分子间不能形成氢键,氢键导致物质的熔沸点升高,所以水的熔沸点高于硫化氢;
(3)①Fe与S形成的化合物为FeS、FeS2,黑色球个数为4、白色球个数=1+8×![]() =2,则黑色球与白色球个数之比为2∶1,所以其化学式为FeS2;
=2,则黑色球与白色球个数之比为2∶1,所以其化学式为FeS2;
② 若晶胞参数为a pm,ρ=![]() =
= g/cm3=
g/cm3=![]() g/cm3。
g/cm3。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】“直接煤燃料电池”能够将煤中的化学能高效、清洁地转化为电能。用熔融Na2CO3作电解质的直接煤燃料电池的工作原理如图。下列有关说法正确的是

A. 该电池的总反应为C+O2=CO2
B. 煤直接燃烧发电比直接煤燃料电池发电的能量利用率高
C. 进入反应室的煤块粉碎成粉末状对反应速率和限度均无影响
D. 电子由电极b沿导线流向电极a,入口A加入的物质为煤粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石墨电极a和石墨电极 电解NaNO3稀溶液的装置如图所示。通电后在两电极附近分别滴加几滴紫色石蕊试液。下列说法不正确的是

A. a电极逸出气体的体积大于b电极的
B. 溶液中的阴离子移向b电极
C. a电极附近溶液呈蓝色,b电极附近溶液呈红色
D. 若将a电极改为铜电极,b电极不变,则通电后a电极无气体逸出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在容积为VL的密闭容器中进行反应:aN(g)![]() bM(g),N、M的物质的量随时间的变化曲线如图所示:
bM(g),N、M的物质的量随时间的变化曲线如图所示:
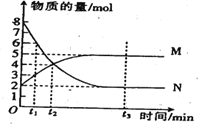
(1)此反应的化学方程式中a:b=________。
(2)t1到t2时,以N的浓度变化表示的平均反应速率为:___________mol·L-1· min-1。
(3)图中哪一时刻反应已经达到限度(____)
A.t1 B.t2 C.t3
(4)其他条件不变时,能使反应速率加快的是(____)
A.升高温度
B.容器体积固定不变时,充入He
C.容器体积固定不变时,充入气体N
D.容器内气体压强不变时,充入Ar
E.容器体积增大为原来的2倍
(5)若N为有色气体,且容器体积恒定,下列结论不能说明上述反应在该条件下已经达到反应限度的是(____)
A.M的消耗速率与N的生成速率之比为1:2
B.容器内气体的压强不再变化
C. N的消耗速率与M的消耗速率之比为2:1
D.容器内气体的质量不再变化
E.N的物质的量浓度不再改变
F.容器内气体的颜色不再改变
G.容器内气体的平均相对分子质量不再变化
H.容器内气体的密度不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关Na2CO3和NaHCO3的叙述中正确的是
A.相同质量的Na2CO3和NaHCO3与足量盐酸作用时,产生的气体质量相同
B.Na2CO3比NaHCO3热稳定性强
C.Na2CO3不能与澄清石灰水反应
D.Na2CO3和NaHCO3均可与NaOH溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无色透明的碱性溶液中,能大量共存的离子组是
A、 Na+、K+、CO32-、NO3- B、Cu2+、Al3+、SO42-、NO3-
C、 K+、Fe2+、NH4+、NO3- D、NH4+、Na+、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下面是4种粒子的结构示意图:
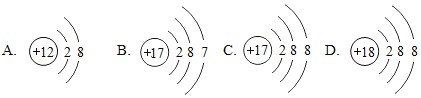
图中粒子共能表示_______种元素,图中表示的阳离子是____________(用离子符号表示),图中A所表示的元素在元素周期表中的位置_____________________________.
(2)在1-18号的短周期主族元素中,表中的字母代表一种元素,回答下列问题:
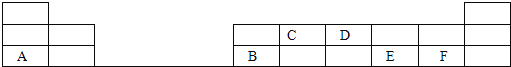
①写出D单质的电子式_____________________;
②写出C的最高价氧化物的结构式_____________________;
③E和F分别形成的气态氢化物中较稳定的是(填写氢化物的化学式)_____________________;
④A最高价氧化物的水化物所含化学键为___________________,其晶体类型为________,其水溶液与B反应的离子方程式为___________________________;
(3)X、Y、Z、M、N、Q皆为短周期主族元素,其原子半径与主要化合价的关系如图所示.下列说法正确的是 (______)
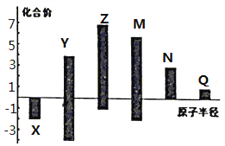
A.金属性:N>Q B.最高价氧化物对应水化物酸性:M>Y>N
C.简单离子半径:Q>N>X D.原子序数:Z>M>X>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A、在一定温度下AgCl水溶液中Ag+ 和Cl—浓度的乘积是一个常数
B、AgCl水溶液的导电性很弱,所以AgCl为弱电解质
C、温度一定时,当AgCl水溶液中Ag+ 和Cl—浓度的乘积等于KSP值时,此溶液为AgCl的饱和溶液
D、向饱和AgCl水溶液中加入盐酸,c(Cl—)增大,KSP值变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的废渣中混有少量的锌粉和氧化铜(其他成分不跟酸反应),跟大量废盐酸接触形成污水,产生公害。若向污水中撒入铁粉且反应后铁粉有剩余,此时污水中一定含有的金属离子是
A.Fe2+、Cu2+ B. Cu2+ 、 H+ C. Zn2+ 、Fe2+ D. Zn2+ 、H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com