
【题目】由下列实验及现象,推出的相应结论正确的是
实验 | 现象 | 结论 |
A.用铂丝蘸取某金属的盐溶液, 在酒精灯火焰上灼烧 | 火焰呈黄色 | 此盐溶液中含有 Na+,不含 K+ |
B.向饱和NaHCO3溶液中加入足量氯水 | 有无色气体产生 | 氯水中含HClO |
C.将足量SO2气体通入石蕊试液中 | 石蕊试液变红色 | SO2水溶液显酸性 |
D.向酸性KMnO4溶液中通入SO2 | 溶液紫色褪去 | SO2具有漂白性 |
A.AB.BC.CD.D
科目:高中化学 来源: 题型:
【题目】近年来,新能源开发和环境保护问题日益引起人们的重视,新型电池是科学家们非常重视的研究方向。用吸附了![]() 的碳纳米管等材料制作的二次电池的原理如图所示。下列说法正确的是( )
的碳纳米管等材料制作的二次电池的原理如图所示。下列说法正确的是( )
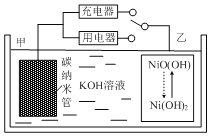
A.碳纳米管的作用只是吸附氢气
B.放电时,乙电极反应为![]()
C.充电时,电池的甲电极与直流电源的正极相连放电
D.电池总反应为H2+2NiO(OH)![]() 2Ni(OH)2
2Ni(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅是一种高密度、柔软的蓝灰色金属。2019年7月23日,铅被列入有害水污染物名录。请回答下列问题。
(1)Pb位于第六周期,与C元素同族。请写出它的外围电子排布式___________,对比以下三种氧化物的熔沸点![]() 、
、![]() 、
、![]() ,从小到大分别为_____________,请解释原因:____________________。
,从小到大分别为_____________,请解释原因:____________________。
(2)铅在自然界主要以方铅矿(PbS)及白铅矿(![]() )的形式存在,也存在于铅矾(
)的形式存在,也存在于铅矾(![]() )中。
)中。![]() 中心原子轨道的杂化类型___________,
中心原子轨道的杂化类型___________,![]() 的空间构型____________。
的空间构型____________。
(3)四乙基铅[![]() ]曾广泛用作汽油中的抗爆剂,由Pb提供空轨道,有机原子团提供孤电子对形成,该化合物中存在化学键类型有_____________
]曾广泛用作汽油中的抗爆剂,由Pb提供空轨道,有机原子团提供孤电子对形成,该化合物中存在化学键类型有_____________
A.金属键 B.离子键 C.共价键 D.配位键
(4)第三代太阳能电池利用有机金属卤化物碘化铅甲胺(![]() )半导体作为吸光材料,
)半导体作为吸光材料,![]() 具有钙钛矿(
具有钙钛矿(![]() )的立方结构,其晶胞如图所示:
)的立方结构,其晶胞如图所示:
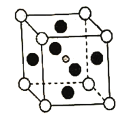
①比较元素电负性:C_________N(填“>”或“<”),比较基态原子第一电离能:C________Pb(填“>”或“<”)
②![]() 晶胞中与金属阳离子(M)距离最近的卤素阴离子(X)形成正八面体结构,则M在晶胞中处于_____________位置,X在晶胞中处于________位置。
晶胞中与金属阳离子(M)距离最近的卤素阴离子(X)形成正八面体结构,则M在晶胞中处于_____________位置,X在晶胞中处于________位置。
③![]() 晶体的晶胞边长为a nm,其晶体密度为d
晶体的晶胞边长为a nm,其晶体密度为d![]() ,则阿伏加德罗常数的值NA的计算表达式为_____________
,则阿伏加德罗常数的值NA的计算表达式为_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式与所述事实相符且正确的是
A.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O=AlO+4NH+2H2O
B.Ca(HCO3)2溶液中加入过量NaOH溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O
C.水玻璃中通入少量的二氧化碳:Na2SiO3+CO2+H2O=2Na++CO32-+H2SiO3↓
D.少量SO2通入漂白粉溶液中:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A.1.8 g NH4+含有的电子数为NA
B.1 L 1 mol·L-1的NaAlO2水溶液中含有的氧原子数为2NA
C.标况下,22.4 L NO与11.2 L O2充分反应后,生成物的分子总数为NA
D.50 mL 18 mol·L-1的浓硫酸与足量的铜片共热,生成SO2的分子数为0.45NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如下图所示(图中有些反应的生成物和反应的条件没有标出)。
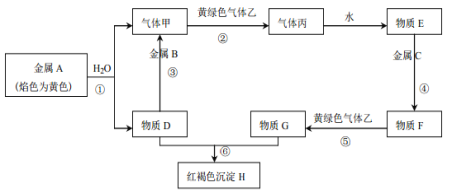
请回答下列问题:
(1)写出 B、乙的化学式:B_______________、乙_______________。
(2)写出下列反应的化学方程式:
反应⑤ ___________________________________________________________;
反应⑥____________________________________________________________。
(3)写出下列反应的离子方程式:
反应①___________________________________________________________;
反应③___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某温度时将nmol·L-1氨水滴入10mLymol·L-1盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示。下列有关说法不正确的是( )
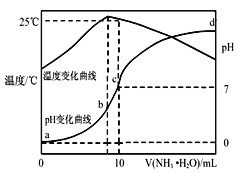
A.y=1.0
B.a点时Kw<1×10-14
C.b点c(NH4+)<c(Cl-)=![]() mol·L-1
mol·L-1
D.25℃时,NH4Cl的水解常数(Kh)可表示为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】B.[实验化学]
丙炔酸甲酯(![]() )是一种重要的有机化工原料,沸点为103~105 ℃。实验室制备少量丙炔酸甲酯的反应为
)是一种重要的有机化工原料,沸点为103~105 ℃。实验室制备少量丙炔酸甲酯的反应为
![]()
实验步骤如下:
步骤1:在反应瓶中,加入14 g丙炔酸、50 mL甲醇和2 mL浓硫酸,搅拌,加热回流一段时间。
步骤2:蒸出过量的甲醇(装置见下图)。
步骤3:反应液冷却后,依次用饱和NaCl溶液、5%Na2CO3溶液、水洗涤。分离出有机相。
步骤4:有机相经无水Na2SO4干燥、过滤、蒸馏,得丙炔酸甲酯。
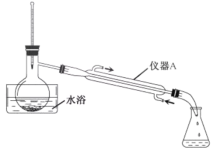
(1)步骤1中,加入过量甲醇的目的是________。
(2)步骤2中,上图所示的装置中仪器A的名称是______;蒸馏烧瓶中加入碎瓷片的目的是______。
(3)步骤3中,用5%Na2CO3溶液洗涤,主要除去的物质是____;分离出有机相的操作名称为____。
(4)步骤4中,蒸馏时不能用水浴加热的原因是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com