
【题目】在稀硫酸和稀硝酸的混合溶液中,加入铜粉。
(1)若将100mL 2mol/L HNO3和100mL 1mol/L H2SO4混合后,加入19.2g 铜粉,微热,充分反应。
①若忽略溶液体积变化,溶液中铜离子物质的量浓度为 mol/L
②生成气体折合成标准状况下体积 L;
③若使铜粉全部溶解,还需加入1mol/L H2SO4 mL
(2)若c(SO![]() )+c(NO
)+c(NO![]() )=5.0 mol·L-1。取200 mL该混合酸,则能溶解铜的最大质量为 g
)=5.0 mol·L-1。取200 mL该混合酸,则能溶解铜的最大质量为 g
【答案】(1)①0.75(2分)②2.24(2分)③200(2分)(2)38.4(3分)
【解析】
试题分析:(1)①n(HNO3)=0.1L×2mol/L=0.2mol,n(H2SO4)=0.1L×1moL/L=0.1moL,n(NO3-)=n(HNO3)=0.2mol,溶液中的氢离子既包括硝酸电离的又包括硫酸电离的:所以n(H+)=0.2moL+2×0.1moL=0.4mol,
n(Cu)=19.2g÷64g/mol=0.3mol,则
3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O
3mol 2mol 8mol
0.3mol 0.2mol 0.8mol
由反应关系可以看出,NO3-过量,H+不足,根据H+计算生成的铜离子,
则生成的n(Cu2+)=0.4mol×3/8=0.15mol,c(Cu2+)=0.15mol÷0.2L=0.75mol/L;
②根据①中分析可知生成NO是0.1mol,折合成标准状况下体积2.24L;
③根据①中分析可知完全溶解铜需要0.8mol氢离子,因此还缺少0.4mol氢离子,则还需要0.2mol硫酸,即还需要200mL1mol/L硫酸;
(2)反应的离子方程式为3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,要使溶解铜的质量最大,则氢离子和硝酸根浓度满足化学计量数即4:1,硝酸全部起氧化剂作用,设硫酸浓度为x,则硝酸浓度为5mol/L-x,溶液中氢离子浓度共:2x+(5mol/L-x),则:[2x+(5mol/Lx)]/(5mol/Lx)=4:1,解得x=3mol/L,硝酸浓度为2mol/L,硝酸的物质的量为:0.2L×2mol/L=0.4mol,根据方程式3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O可知溶解铜是0.6mol,质量是0.6mol×64g/mol=38.4g。


科目:高中化学 来源: 题型:
【题目】有机物G(分子式为C13H18O2)是一种香料,下图是该香料的一种合成路线。
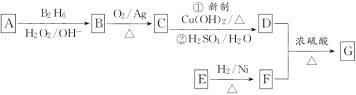
已知:
①E能够发生银镜反应,1 mol E能够与2 mol H2完全反应生成F
②R—CH=CH2![]() R—CH2CH2OH
R—CH2CH2OH
③有机物D的摩尔质量为88 g·mol-1,其核磁共振氢谱有3组峰
④有机物F是苯甲醇的同系物,苯环上只有一个无支链的侧链
回答下列问题:
(1)用系统命名法命名有机物B:________。
(2)E的结构简式为________。
(3)C与新制Cu(OH)2反应的化学方程式为________。
(4)有机物C可与银氨溶液反应,配制银氨溶液的实验操作为______________________。
(5)已知有机物甲符合下列条件:
①为芳香族化合物
②与F互为同分异构体
③能被催化氧化成醛
符合上述条件的有机物甲有________种。其中满足苯环上有3个侧链,且核磁共振氢谱有5组峰,峰面积之比为6∶2∶2∶1∶1的有机物的结构简式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列数量的各物质所含原子数按由大到小顺序排列的是
①0.5 mol NH3 ②标况下22.4 L He ③18 g水 ④0.8 mol Na3PO4
A. ①④③② B. ④③②① C. ②③④① D. ④③①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验的说法不正确的是( )
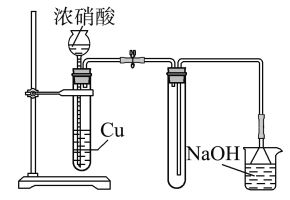
A.用广泛pH试纸测得0.051 mol·L-1H2SO4溶液的pH=1
B.某气体制备装置如上图,该装置可减少污染性气体的泄
漏,且有利于收集到空气含量较低的气体
C.在分液操作中,当试液分层后,打开旋塞,将下层液体放出,然后关闭旋塞,将上层液体从上口倒出
D.10 mL溴水与5 mL正己烷混合,在光照下振荡后静置,当试液分为上、下两层且几乎无色时,用玻璃棒蘸取浓氨水伸入液面上方,可观察到有白烟生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究性学习小组利用下列有关装置进行探究实验,回答相关问题。
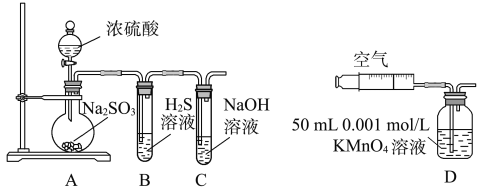
(1)写出A中反应的化学方程式:____________________。
(2)实验时,旋开装置A中分液漏斗的旋塞,发现液体流出缓慢,最终停止,其可能的原因是__________________________。
(3)装置B中的溶液出现浑浊,该实验证明SO2具有______性。
(4)实验后,测定装置C中溶液呈碱性。溶液为什么呈碱性呢?大家有不同意见:①是生成的Na2SO3水解;②是氢氧化钠剩余。请设计实验方案证明哪种意见成立。选用下列试剂进行实验:Na2SO3溶液、酚酞溶液、氯水、BaCl2溶液、稀硫酸。
实验步骤 | 实验操作 | 预期现象与结论 |
(5)另一小组利用装置D进行实验:用注射器向装置D共注入V mL实验室制备SO2后的空气,当溶液刚好褪色,停止实验。该小组的实验目的是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校研究性学习小组的同学学习完氮的有关性质之后,对氮元素的氢化物和氧化物的性质进行了更深入的研究。
Ⅰ.NH3的性质探究
(1)实验室制取氨气的化学方程式为_______________________。
(2)某同学模仿排饱和食盐水收集氯气的方法,想用排饱和氯化铵溶液的方法收集氨气。你认为他能否达到目的?________(填“能”或“否”),理由是_____________________________。
(3)该小组的同学设计了如下图所示的实验装置(夹持及尾气处理装置未画出),探究氨气的还原性。
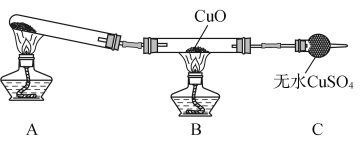
①该装置在设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是______________________。
②利用改进后的装置进行实验,观察到CuO变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体。则氨气与CuO反应的化学方程式为_______________________________。
③有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O。已知:Cu2O是一种碱性氧化物,在酸性溶液中,Cu+→Cu+Cu2+。请设计一个简单的实验检验该红色物质中是否含有Cu2O:_____________________________。
Ⅱ.NO2的性质探究
该小组的同学还设计了如图所示装置,用以制取NO2并验证NO2能否支持木条燃烧(忽略N2O4的存在,图中铁架台等夹持仪器均已略去)。已知:2Cu(NO3)2![]() 2CuO+4NO2↑+O2↑。
2CuO+4NO2↑+O2↑。
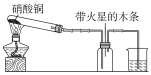
(4)当集气瓶中充满红棕色气体时,木条复燃了。有的同学得出“NO2能支持木条的燃烧”的结论。你认为这一结论是否正确?________(填“正确”或“不正确”),理由是___________________________。
(5)NH3与NO2在一定条件下可以反应生成无污染性气体,体现了NH3的还原性,化学方程式为___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A为淡黄色固体,R是地壳中含量最多的金属元素的单质,T为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体,C、F是无色无味的气体,H是白色沉淀,W溶液中滴加KSCN溶液出现红色。
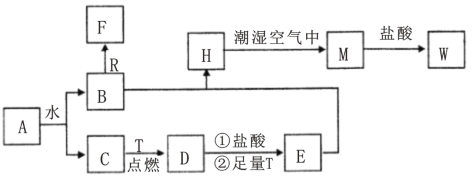
(1)物质D的化学式为___________,E化学式为___________;
(2)点燃气体F前必须先_________________________;
(3)H在潮湿空气中变成M的实验现象是_______________,化学方程式为_______________,其反应类型是 反应(填基本反应类型)。
(4)B和R在溶液中反应生成F的离子方程式为____________________,该反应属 反应 (填基本反应类型)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com