
| A、4种 | B、6种 |
| C、10种 | D、12种 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
 已知溶液中,还原性为HSO3->I-,氧化性为IO3->I2>SO42-.
已知溶液中,还原性为HSO3->I-,氧化性为IO3->I2>SO42-.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、所有的复分解反应都是非氧化还原反应 |
| B、能与酸反应的氧化物,一定是碱性氧化物 |
| C、同一元素不可能既表现金属性,又表现非金属性 |
| D、以共价键形成的单质中只存在非极性键,以共价键形成的化合物中只存在极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 弱酸 | H2CO3 | H2SO3 | HClO |
| 电离平衡常数 (25℃) |
K1=4.30×10-7 | K1=1.54×10-2 | K=2.95×10-8 |
| K2=5.61×10-11 | K2=1.02×10-7 |
| A、相同温度时三种溶液的pH关系:Na2CO3>NaClO>Na2SO3 |
| B、ClO-+H2O+CO2→HClO+HCO3- |
| C、2ClO-+SO2+H2O→2HClO+SO32- |
| D、等体积、等物质的量浓度的HClO 和Na2CO3混合后溶液呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl2与H2O反应:Cl2+H2O═2H++Cl-+ClO- |
| B、向氯化铁溶液中加氢碘酸能使溶液变为无色 |
| C、向NaClO溶液中通入少量的CO2:2ClO-+CO2+H2O═2HClO+CO32- |
| D、200mL 2mol/L的FeBr2溶液中通入11.2L标准状况下的Cl2:4Fe2++2Br-+5Cl2═4Fe3++3Br2+10Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、6种 |
| B、7 种 |
| C、8 种 |
| D、9种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ca2+、K+、CO32-、Cl- |
| B、K+、NH4+、HCO3-、OH- |
| C、H+、Fe2+、ClO-、SO42- |
| D、Na+、Ba2+、OH-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、PM2.5颗粒直径约是原子直径的2.5倍 |
| B、淀粉、蔗糖、氨基酸在一定条件都能发生水解反应 |
| C、植物油通常能和氢氧化钠溶液发生反应 |
| D、应该倡议禁止向绿色食品中添加任何化学物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
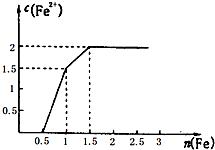 通过对模型、图形、图表的观察,能获取有关信息是化学学习的一种重要能力.按要求回答下列问题.
通过对模型、图形、图表的观察,能获取有关信息是化学学习的一种重要能力.按要求回答下列问题.| 元素编号/元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| X | 3.44 | 2.55 | 0.98 | 2.04 | 2.19 | 3.16 | 0.93 | 3.04 | 1.61 | |
| 常见化合价 | 最高价 | +4 | +1 | +3 | +1 | +3 | ||||
| 最低价 | -2 | -4 | -3 | -1 | -3 | |||||
| 物质/20℃时溶解度(g/100g溶剂) | AgNO3 | Ba(NO3)2 | AgCl | BaCl2 |
| 水中 | 216 | 9.02 | 1.9×10-14 | 35.8 |
| 液氨 | 86 | 97.2 | 0.8 | 0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com