
在标准状况下,H2和O2混合气体A L,引爆冷却到原始状态时,体积减少为B L,则原混合气体中H2占有的体积可能为多少L?
| 有关混合物反应的计算. | |
| 分析: | 反应方程式为2H2 +O2 |
| 解答: | 解:反应前后气体的体积不会为:AL﹣BL=(A﹣B)L,根据差量法可得: 2H2 +O2 2 1 3
当氢气过量时,氧气完全反应,混合物中氧气的体积为: 当氧气过量时,氢气完全反应,则混合气体中氢气的体积为: 答:原混合气体中H2占有的体积可能为 ( |
| 点评: | 本题考查了混合物反应的计算,题目难度中等,明确发生反应原理为解答关键,注意差量法在化学计算或者的应用方法,试题考查了学生的分析能力及化学计算能力. |


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
室温下向10mL pH=3的醋酸溶液中加入水稀释后,下列说法正确的是 ( )
A.溶液中导电粒子的数目增加,导电性增强
B.醋酸的电离程度增大,减小
C.再加入10mL pH=11 NaOH溶液,混合液pH=7
D.溶液中由水电离出的=1×10-11 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
部分弱酸的电离平衡常数如下表:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25 ℃) | Ki=1.77×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
下列选项错误的是( )
①2CN-+H2O+CO2===2HCN+CO
②2HCOOH+CO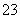 ===2HCOO-+H2O+CO2↑
===2HCOO-+H2O+CO2↑
③中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者
④等体积、等浓度的HCOONa和NaCN溶液中所含离子总数前者小于后者
A.①② B.②③
C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
NA代表阿伏加德罗常数,下列说法正确的是()
| A. | 2.3g钠由原子变成离子时,得到的电子数为0.1NA | |
| B. | 0.2NA个硫酸分子与19.6g磷酸含有相同的氧原子数 | |
| C. | 28g氮气所含有的原子数为NA | |
| D. | NA个氧分 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在20℃时一刚性容器内部有一不漏气且可滑动的活塞将容器分隔成左、右室两室.左室充入N2,右室充入H2和O2,活塞正好停留离左端1/5处(如图a)然后点燃引爆H2和O2混合器,活塞先左弹(设容器不漏气),恢复至原来温度,活塞恰好停在中间(如图b),水蒸气的体积可忽略,则反应前H2和O2的体积比可能是()
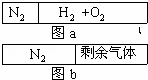
| A. | 7:1 | B. | 1:3 | C. | 1:1 | D. | 3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是()
| A. | 铜能导电,所以铜是电解质 | |
| B. | BaSO4难溶于水,但BaSO4属于强电解质 | |
| C. | 液态HCl不能导电,所以HCl是非电解质 | |
| D. | 氯气的水溶液能导电,氯气是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式正确的是()
| A. | 铁和足量稀硝酸反应 Fe+2H+═Fe2++H2↑ | |
| B. | 氯化铁溶液滴入沸水 Fe3++3H2O | |
| C. | 硝酸银溶液中滴入食盐水 Cl﹣+Ag+═AgCl↓ | |
| D. | 氯气通入烧碱溶液 Cl2+2OH﹣═Cl﹣+ClO﹣+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
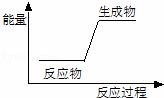 下列反应前后物质的总能量变化可用如图表示的是
下列反应前后物质的总能量变化可用如图表示的是
A.H﹣F═H+F
B.Mg+2H+=Mg2++H2↑
C.2Na+2H2O=2Na++2OH-+ H2↑
D.HNO3+NaOH=NaNO3+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C都是金属;B与C混合,只有C能被盐酸溶解;A与B组成原电池时,A为电池的正极。则A、B、C三种金属的活动性顺序为
A.A>B>C B.A >C>B
>C>B
C.C>B>A D.B>C>A
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com