
| 元素代号 | 相关信息 |
| A | A的单质能与冷水剧烈反应,得到强碱性溶液 |
| B | B的原子最外层电子数是其内层电子数的三倍 |
| C | 是地壳中含量最高的金属元素 |
| D | A、B、D组成的化合物X是84消毒剂的主要成分 |
| E | 所有有机物中都含有E元素 |
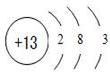 .
.分析 短周期主族元素,A的单质能与冷水剧烈反应,得到强碱性溶液,则A为Na;B的原子最外层电子数是其内层电子数的三倍,可知2个电子层,最外层电子数为6,B为O;
C是地壳中含量最高的金属元素,则C为Al;A、B、D组成的化合物X是84消毒剂的主要成分NaClO,可知D为Cl;所有有机物中都含有E元素,则E为C,然后结合元素周期律及元素化合物知识来解答.
解答 解:短周期主族元素,A的单质能与冷水剧烈反应,得到强碱性溶液,则A为Na;B的原子最外层电子数是其内层电子数的三倍,可知2个电子层,最外层电子数为6,B为O;
C是地壳中含量最高的金属元素,则C为Al;A、B、D组成的化合物X是84消毒剂的主要成分NaClO,可知D为Cl;所有有机物中都含有E元素,则E为C,
(1)E元素周期表中的位置第2周期、第IVA族;C的原子结构示意图为 ,故答案为:第2周期、第IVA族;
,故答案为:第2周期、第IVA族; ;
;
(2)X的化学式为NaClO,故答案为:NaClO;
(3)电子层越多离子半径越大,具有相同电子的离子原子序数大的离子半径小,则A、B、D三种元素形成的简单离子半径由大到小的顺序为Cl->O2->Na+,
故答案为:Cl->O2->Na+;
(4)A、B形成的一种原子个数比为1:1化合物的化学式为Na2O2,故答案为:Na2O2;
(5)A在真空高压下能与由元素D、E组成化合物ED4反应生成两种固体物质,其中一种是自然界中硬度最大的物质,可知Na与四氯化碳反应生成氯化钠和C,该化学反应为4Na+CCl4$\frac{\underline{\;真空高压\;}}{\;}$4NaCl+C,故答案为:4Na+CCl4$\frac{\underline{\;真空高压\;}}{\;}$4NaCl+C.
点评 本题考查位置、结构与性质,为高频考点,把握元素的位置、性质及元素化合物知识为解答的关键,侧重分析与应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:实验题
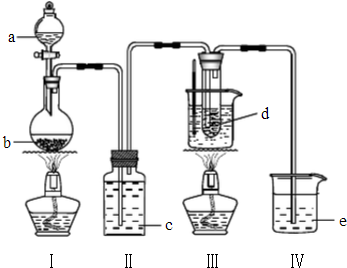 氯气与碱溶液反应时,在低温和稀碱溶液中主要产物是ClO-和Cl-,在75℃以上和浓碱溶液中主要产物是ClO-和Cl-.研究小组用以下实验装置制取氯酸钾(KClO3)并测定溶度.
氯气与碱溶液反应时,在低温和稀碱溶液中主要产物是ClO-和Cl-,在75℃以上和浓碱溶液中主要产物是ClO-和Cl-.研究小组用以下实验装置制取氯酸钾(KClO3)并测定溶度.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 64gCu被氧化,失去的电子数一定为2NA | |
| B. | 室温下,pH=13的氨水中,由水电离的OH-数为0.1NA | |
| C. | 在标准状况下,22.4LC4H10中共价键数目为13NA | |
| D. | 200mL1mol/LFe2 ( SO4)3 溶液中,SO42-离子数是0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 相关实验 | 预期目的 | |
| A | 相同温度下,将等质量的大理石块、大理石粉末分别加入等体积、等浓度的盐酸和醋酸中,观察气泡产生的快慢 | 验证固体接触面积对化学反应速率的影响 |
| B | 可逆反应FeCl3(aq)+3KSCN(aq)?Fe(SCN)3(aq)+3KCl(aq)建立平衡后,在其它条件不变时,加入KCl固体,观察体系颜色的变化 | 验证浓度对化学平衡的影响 |
| C | 室温下,向BaSO4悬浊液中加入饱和Na2CO3溶液,过滤后,再向沉淀中加入盐酸,沉淀部分溶解 | 验证BaSO4和BaCO3的Ksp的相对大小 |
| D | 相同温度下,两支试管中装有等体积、等浓度的H2O2溶液,向其中分别加入少量FeCl3固体和少量的MnO2固体 | 验证不同催化剂对H2O2分解速率的影响 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应的热化学方程式为2NH4Cl+Ba(OH)2═BaCl2+2NH3•H2O;△H>0 | |
| B. | 反应物的总能量低于生成物的总能量 | |
| C. | 氯化铵与氢氧化钡的反应为放热反应 | |
| D. | 该反应中,化学能全部转化为热能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制氯水中既有分子,又有离子 | |
| B. | 久置的氯水可以使干燥的有色布条褪色 | |
| C. | 新制氯水中滴加硝酸银溶液,没有任何现象 | |
| D. | 新制氯水在光照条件下,可以产生气体,该气体是氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
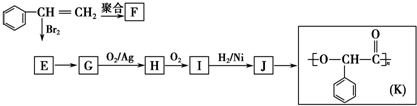
 ;I的结构简式是
;I的结构简式是 .
.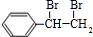 +2NaOH$→_{△}^{水}$
+2NaOH$→_{△}^{水}$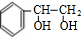 +2NaBr;反应类型属于水解反应.
+2NaBr;反应类型属于水解反应. +H2 $\stackrel{一定条件}{→}$
+H2 $\stackrel{一定条件}{→}$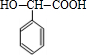 ;反应类型属于加成反应.
;反应类型属于加成反应.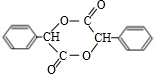 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com