
Ⅰ.为了将混有K2SO4、MgSO4的KNO3固体提纯,并制得纯净的KNO3溶液,某学生设计如下实验方案:
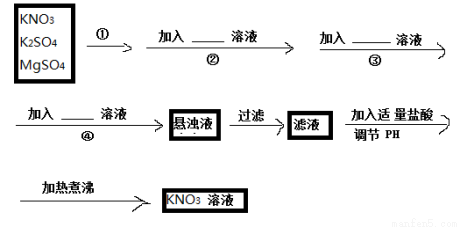
(1)操作①为_____________________。
(2)操作②~④加入的试剂依次可以为:__________________________
(3)如何判断SO42-已除尽?
(4)实验过程中产生的多次沉淀________(填“需要”或“不需要”)多次过滤,其理由是______________
(5)该同学的实验设计方案是否严密?请说明理由:_________________。
Ⅱ.实验室需要 0.1mol/L的 H2SO4溶液980mL,欲用 98%、密度为1.84g/cm3的浓硫酸配制。
(1)需要的玻璃仪器除了量筒、烧杯、玻璃棒外还需要________________
(2)应用量取的浓硫酸体 积为 mL。
积为 mL。
(3)试分析下列操作对所配溶液的浓度有何影响(填: 偏高、偏低、或无影响,下同)
①量取浓硫酸时眼睛俯视量筒刻度线,会导致所配溶液浓度会 ;
②未冷却到室温就移液、定容 。
③移液前容量瓶中有水 。
④定容时,眼睛仰视刻度线,所配溶液浓度会 。
 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源:2016-2017学年河北省高一上11月月考化学卷(解析版) 题型:推断题
某固体混合物可能由KCl、NaNO3、K2SO4、CuCl2、CaCl2、K2CO3中的一种或几种混合而成,为鉴定其组成,依次进行如下实验:
(1)混合物中加入足量水得一无色透明溶液,
(2)上述溶液中滴加 BaCl2有白色沉淀产生,
(3)过滤,然后向上述白色沉淀加盐酸时,沉淀全部溶解,
(4)往滤液中加AgNO3溶液时有白色沉淀产生且白色沉淀不溶于稀硝酸。
①试判断:肯定存在的物质有_________;肯定不存在的物质有________;可能存在的物质有_________。
②写出第(3)步反应的离子方程式___________________。
查看答案和解析>>
科目:高中化学 来源:2017届山西省晋商四校高三上11月联考化学试卷(解析版) 题型:选择题
有关能量的判断或表示方法正确的是 ( )
A.2H2(g)+O2(g) =2H2O(g)ΔH=—483.6 kJ·mol-1,则H2燃烧热为241.8 kJ·mol-1
B.从C(石墨,s)= C(金刚石,s) ΔH=+1.9 kJ/mol,可知:金刚石比石墨更稳定
C.等质量的硫蒸气和硫固体分别完全燃烧,后者放出热量更多
D.化学反应中的能量变化,通常表现为热量的变化
查看答案和解析>>
科目:高中化学 来源:2016-2017学年西藏拉萨中学高二上月考三化学卷(解析版) 题型:选择题
控制适合的条件,将反应2Fe3++2I- 2Fe2++I2设计成如图所示的原电池。下列判断不正确的是:
2Fe2++I2设计成如图所示的原电池。下列判断不正确的是:

A.反应开始时,乙中石墨电极上发生氧化反应
B.反应开始时,甲中石墨电极上Fe3+被还原
C.电流计读数为零时,反应达到化学平衡状态
D.电流计读数为零后,在甲中溶入FeCl2固体,乙中石墨电极为负极
查看答案和解析>>
科目:高中化学 来源:2016-2017学年西藏拉萨中学高二上月考三化学卷(解析版) 题型:选择题
表示下列用途或变化的离子方程式不正确的是:
A.泡沫灭火器灭火原理:Al3++3HCO3-===3CO2↑+Al(OH)3↓
B.纯碱代替洗涤剂洗涤餐具:CO32-+H2O HCO3-+OH-
HCO3-+OH-
C.明矾净水原理:Al3++3H2O Al(OH)3(胶体)+3H+
Al(OH)3(胶体)+3H+
D.NaHCO3的水【解析】
HCO3-+H2O H3O++ CO32-
H3O++ CO32-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津静海一中等六校高一上期中化学卷(解析版) 题型:选择题
下图为某市售盐酸试剂瓶标签上的部分数据。下列说法正确的是:

A. 足量的该盐酸与1molFe反应生成22.4L H2
B. 该盐酸的物质的量浓度为11.8mol/L
C. 该盐酸与等体积的水混合后所得溶液的物质的量浓度为5.9mol/L
D. 配制80mL 5.9mol/L 的盐酸需用量筒量取40mL该盐酸
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津静海一中等六校高一上期中化学卷(解析版) 题型:选择题
宋代著名法医学家宋慈的《洗冤集录》中有―银针验毒的记载,“银针验毒”的原理是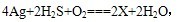 下列说法正确的是( )
下列说法正确的是( )
A.X的化学式为AgS B.银针验毒时,空气中氧气失去电子
C.反应中Ag和H2S均是还原剂 D.每生成1molX,反应转移2mol e-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一上期中化学卷(解析版) 题型:实验题
(1)用托盘天平称取NaOH固体____________g。称量NaOH固体需注意:因NaOH具有腐蚀性,在称量时需用烧杯盛装NaOH固体;称量必须迅速,其原因是_________________________。
(2) 接下来完成此实验你将用到的仪器有玻璃棒、烧杯、_________________。
而某同学提出只需再选择带刻度的500 mL烧杯和玻璃棒,即可配制500 mL 0.10 mol/L的NaOH溶液;你对此方案的评价是_______________________。
(3) 若你从所配的溶液中取出50 mL于一试剂瓶中,请给它贴上标签,标签的内容是_________;
若再从中取出10 mL溶液加水稀释至20 mL,则此时溶液的物质的量浓度为____________。
(4) 下列操作对所配溶液浓度没有影响的是_______。
A.称量时已观察到NaOH表面潮湿 |
B.将烧杯中溶解后的溶液立即注入容量瓶,然后再添加蒸馏水至刻度线 |
C.摇匀定容后,又用胶头滴管向容量瓶中滴加蒸馏水至刻度线 |
D.配制溶液前用蒸馏水润洗容量瓶,但未烘干 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西大学附中高二上期中化学卷(解析版) 题型:选择题
一定量的混合气体在密闭容器中发生反应:mA(g)+nB(g) pC(g)达到平衡时,维持温度不变,将气体体积缩小到原来的1/2,当达到新
pC(g)达到平衡时,维持温度不变,将气体体积缩小到原来的1/2,当达到新 的平衡时,气体C的浓度变为原平衡时的1.9倍
的平衡时,气体C的浓度变为原平衡时的1.9倍 ,则下列说法正确的是( )
,则下列说法正确的是( )
A.m+n>p B.m+n<p
C.平衡向正反应方向移动 D.C的质量分数增加
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com