
A.1.2 mol B.1.5 mol C.1.8 mol D.2.5 mol
解析:依题意可写出如下关系式
CO2 + H2 ![]() CO + H2O
CO + H2O
起始1: 1 mol 3 mol 0 0
平衡1:(1-0.75)mol (3-0.75)mol 0.75 mol 0.75 mol
起始2: 1 mol 9 mol 0 0
平衡2: (1-x)mol (9-x)mol x mol x mol
“起始2”相对“起始1”H2的量增加了,所以“平衡2”可看作是“平衡1”正向移动的结果,即x>0.75 mol,所以生成物之和大于1.5 mol,由此可排除A、B两选项。
C、D两选项如何确定呢?根据“大于零原则”(即可逆反应中任一组分的量大于零),可建立如下关系式:(1-x)>0且(9-x)>0,由此可得:x<1,即生成物之和小于2。所以C选项为正确答案。
答案:C


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:
在一个密闭容器中充入一种气态烃和足量的氧气,用电火花点燃,完全燃烧后,容器内气体体积保持不变(均在120℃和相同的压强下测定),这种气态烃可能是( )
A.CH4 B.C2H6 C.C2H4 D.C3H6
查看答案和解析>>
科目:高中化学 来源:2012届山西省山大附中高三3月月考理综部分(带解析) 题型:填空题
(16分)氨是一种重要的化工原料,氨的合成和应用是当前的重要研究内容之一。
(1)一定条件下,在一个密闭容器中充入气体:N2 2mol、H2 6mol,达平衡后N2的转化率为50%,同时放热92.3KJ。该反应的热化学方程式为:______________________________。
(2)传统哈伯法合成氨工艺中相关的反应式为:N2+3H2 2NH3。
2NH3。
①该反应的平衡常数K的表达式为:K=______________。升高温度,K值______(填“增大”“减小”或“不变”)。
②不同温度、压强下,合成氨平衡体系中NH3的物质的量分数见下表(N2和H2的起始物质的量之比为1∶3)。分析表中数据, (填温度和压强)。时H2转化率最高,实际工业生产中不选用该条件的主要原因是 。
③下列关于合成氨说法正确是 (填字母)
A.使用催化剂可以提高氮气的转化率
B.寻找常温下的合适催化剂是未来研究的方向
C.由于ΔH<0、ΔS>0,故合成氨反应一定能自发进行
(3)最近美国Simons等科学家发明了不必使氨先裂化为氢就可直接用于燃料电池的方法。其装置为用铂黑作为电极,加入电解质溶液中,一个电极通入空气,另一电极通入氨气。其电池反应为4NH3+3O2=2N2+6H2O,你认为电解质溶液应显 性(填“酸性”、“中性"、“碱性”),写出负极电极反应式 。
(4)工业上净化处理铬污染方法之一是:将含K2Cr2O7酸性废水放入电解槽内,加入适量的NaCl,以Fe和石墨为电极进行电解。经过一段时间后,生成Cr(OH)3和Fe(OH)3沉淀除去(已知Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31)。
已知电解后的溶液中c(Fe3+)为2.0×10-13mol/L,则溶液中c(Cr3+)为 mol/L。
查看答案和解析>>
科目:高中化学 来源:2013届广东省高二下学期期中考试理科化学试卷(解析版) 题型:选择题
在一个密闭容器中充入一种气态烃和足量的氧气,用电火花点燃,完全燃烧后,容器内气体体积保持不变(均在120℃和相同的压强下测定),这种气态烃可能是( )
A.CH4 B.C2H6 C.C2H4 D.C3H6
查看答案和解析>>
科目:高中化学 来源:2011-2012学年山西省高三3月月考理综部分(解析版) 题型:填空题
(16分)氨是一种重要的化工原料,氨的合成和应用是当前的重要研究内容之一。
(1)一定条件下,在一个密闭容器中充入气体:N2 2mol、H2 6mol,达平衡后N2的转化率为50%,同时放热92.3KJ。该反应的热化学方程式为:______________________________。
(2)传统哈伯法合成氨工艺中相关的反应式为:N2+3H2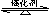 2NH3 。
2NH3 。
①该反应的平衡常数K的表达式为:K=______________。升高温度,K值______(填“增大”“减小”或“不变”)。
②不同温度、压强下,合成氨平衡体系中NH3的物质的量分数见下表(N2和H2的起始物质的量之比为1∶3)。分析表中数据, (填温度和压强)。时H2转化率最高,实际工业生产中不选用该条件的主要原因是 。

③下列关于合成氨说法正确是 (填字母)
A.使用催化剂可以提高氮气的转化率
B.寻找常温下的合适催化剂是未来研究的方向
C.由于ΔH<0、ΔS>0,故合成氨反应一定能自发进行
(3)最近美国Simons等科学家发明了不必使氨先裂化为氢就可直接用于燃料电池的方法。其装置为用铂黑作为电极,加入电解质溶液中,一个电极通入空气,另一电极通入氨气。其电池反应为4NH3+3O2=2N2+6H2O,你认为电解质溶液应显 性(填“酸性”、“中性"、“碱性”),写出负极电极反应式 。
(4)工业上净化处理铬污染方法之一是:将含K2Cr2O7酸性废水放入电解槽内,加入适量的NaCl,以Fe和石墨为电极进行电解。经过一段时间后,生成Cr(OH)3和Fe(OH)3沉淀除去(已知Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31)。
已知电解后的溶液中c(Fe3+)为2.0×10-13mol/L,则溶液中c(Cr3+)为 mol/L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com