
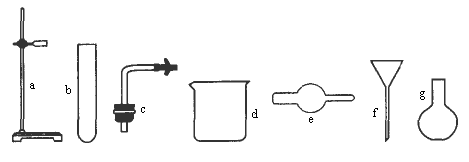
实验室可以用如图所示仪器连接起来,制备纯净的CO2并测定其相对分子质量.

现用含有少量硫化亚铁的大理石和盐酸反应制备CO2气体,实验步骤如下:
(1)将橡皮塞B塞在烧瓶A的瓶口,并用橡皮筋套在烧瓶的瓶颈处以标记橡皮塞所塞入瓶颈的深度,准确称其质量为m1 g.
(2)连接制备和净化气体的装置,其连接顺序是:________接________,________接________,________接________,,________接________.
(3)将导管G插入烧瓶A中用向________(填“上”或“下”)排空气法收集二氧化碳气体.检验二氧化碳气体已经充满烧瓶的方法是________.若经检验,二氧化碳气体已经充满烧瓶,迅速用橡皮塞塞好烧瓶瓶口,并称其质量为m2 g.
(4)将瓶口橡皮塞取下,向烧瓶中注水至标记线,再将水小心地倒入量筒,测量出水的体积为V1 mL;将该体积换算成标准状况时的体积为V2 mL.请写出二氧化碳的相对分子质量的计算式:________.若不将气体净化和干燥,所测定的二氧化碳相对分子质量的数值将会________(填“偏高”或“偏低”),其理由是________.
(5)若没有现成的CO2气体发生器,请你选用如图中的部分仪器,装配成一个简易并且能随用、随关、随停的CO2气体发生装置.应选用的仪器是________(填编号).
|
【解答】(2)g,a,b,c,d,e,f,h(或g,c,d,a,b,e,f,h);(3)上,用燃着的木条放在瓶口,若火焰熄灭,则证明CO2已经充满;(4) 【巧解导析】因反应后产生的CO2中含HCl,H2S,H2O(气)等杂质,需要除去,其操作规律一般是先进行溶液的除杂操作,后进行干燥.其原因是气体通过溶液时(浓H2SO4除外)将带出水蒸气,干燥剂可除去这些水蒸气.故装置的连接顺序为g→a→b→c→d→e→f→h或g→c→d→a→b→e→f→h.又因m1=瓶重+空气,m2=瓶重+CO2,故m2-m1为瓶中CO2与空气的质量差.由题意知瓶中气体的物质的量= |
|
【巧解点悟】解实验题的关键要弄清实验的目的及原理,根据实验的目的答题.此类题若不仔细分析,没有形成一定的分析思路则很易做错. |


 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
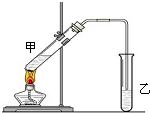 俗话说,“陈酒老醋特别香”,其原因是酒在储存过程中生成了有香味的乙酸乙酯,在实验室里我们也可以用如图所示的装置来模拟该过程.请回答下列问题:
俗话说,“陈酒老醋特别香”,其原因是酒在储存过程中生成了有香味的乙酸乙酯,在实验室里我们也可以用如图所示的装置来模拟该过程.请回答下列问题:查看答案和解析>>
科目:高中化学 来源:2011-2012学年安徽省亳州市高一下学期期末考试化学试卷(带解析) 题型:实验题
(12分) 在实验室,可以用如图所示的装置制取乙酸乙酯。回答下列问题:
(1)右侧试管中的盛放的是 ,导气管的下端不能插入液面以下,其目的是 。
(2)写出实验室制取乙酸乙酯的化学反应方程式 ,该反应的类型是 。
(3)该反应是典型的可逆反应,若不把生成的乙酸乙酯及时蒸馏出来,反应一段时间后,就会达到化学平衡状态。下列能说明该反应已达到化学平衡状态的有(填序号) 。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水;
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸;
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸;
④正反应的速率与逆反应的速率相等;
⑤混合物中各物质的浓度不再变化。
查看答案和解析>>
科目:高中化学 来源:2014届安徽省亳州市高一下学期期末考试化学试卷(解析版) 题型:实验题
(12分) 在实验室,可以用如图所示的装置制取乙酸乙酯。回答下列问题:
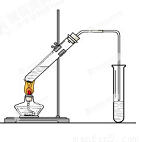
(1)右侧试管中的盛放的是 ,导气管的下端不能插入液面以下,其目的是 。
(2)写出实验室制取乙酸乙酯的化学反应方程式 ,该反应的类型是 。
(3)该反应是典型的可逆反应,若不把生成的乙酸乙酯及时蒸馏出来,反应一段时间后,就会达到化学平衡状态。下列能说明该反应已达到化学平衡状态的有(填序号) 。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水;
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸;
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸;
④正反应的速率与逆反应的速率相等;
⑤混合物中各物质的浓度不再变化。
查看答案和解析>>
科目:高中化学 来源: 题型:
在实验室,可以用如图所示的装置制取乙酸乙酯。
回答下列问题:
(1)右侧试管中的盛放的是 ,
导气管的下端不能插入液面以下,其目的是 。(2)写出实验室制取乙酸乙酯的化学反应方程式 ,该反应的类型是 。
(3)该反应是典型的可逆反应,若不把生成的乙酸乙酯及时蒸馏出来,反应一段时间后,就会达到化学平衡状态。下列能说明该反应已达到化学平衡状态的有(填序号) 。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水;
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸;
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸;
④正反应的速率与逆反应的速率相等;
⑤混合物中各物质的浓度不再变化。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com