
| A£® | ÓĆ¹żĀĖµÄ·½·ØæÉŅŌ³żČ„Ź³ŃĪĖ®ÖŠµÄÄąÉ³ | |
| B£® | ¾Ę¾«µĘ¼ÓČČÉÕĘæŹ±²»ÓƵęŹÆĆŽĶų | |
| C£® | ĀČ»ÆĒāĘųĢåÄÜŹ¹øÉŌļµÄĄ¶É«ŹÆČļŹŌÖ½±äŗģ | |
| D£® | Ź¢·ÅĒāŃõ»ÆÄĘČÜŅŗµÄ²£Į§Ę棬æÉŅŌŹ¹ÓĆĻš½ŗČū»ņ²£Į§Čū |
·ÖĪö A£®ÄąÉ³²»ČÜÓŚĖ®£»
B£®ÉÕĘæ²»ÄÜÖ±½Ó¼ÓČČ£»
C£®øÉŌļµÄĀČ»ÆĒā²»ÄܵēĄė³öĒāĄė×Ó£»
D£®²»ÄÜÓĆ²£Į§Čū£®
½ā“š ½ā£ŗA£®ÄąÉ³²»ČÜÓŚĖ®£¬æÉÓĆ¹żĀĖµÄ·½·Ø·ÖĄė£¬¹ŹAÕżČ·£»
B£®ÉÕĘæ²»ÄÜÖ±½Ó¼ÓČČ£¬Ó¦µęŹÆĆŽĶų£¬¹ŹB“ķĪó£»
C£®øÉŌļµÄĀČ»ÆĒā²»ÄܵēĄė³öĒāĄė×Ó£¬ČÜŅŗ³ŹĖįŠŌ£¬æÉŹ¹ŹŖČóµÄĄ¶É«ŹÆČļŹŌÖ½±äŗģ£¬¹ŹC“ķĪó£»
D£®ĒāŃõ»ÆÄĘŗĶ²£Į§µÄÖŠµÄ¶žŃõ»Æ¹č·“Ó¦£¬µ¼ÖĀ²£Į§Čū“ņ²»æŖ£¬²»ÄÜÓĆ²£Į§Čū£¬¹ŹD“ķĪó£®
¹ŹŃ”A£®
µćĘĄ ±¾Ģā×ŪŗĻæ¼²éĪļÖŹµÄ·ÖĄė”¢Ģį“攢ŅĒĘ÷µÄŹ¹ÓĆŗĶŅ©Ę·µÄ±£“ę£¬ĪŖøßæ¼³£¼ūĢāŠĶ£¬²ąÖŲæ¼²éѧɜµÄ·ÖĪöÄÜĮ¦ŗĶŹµŃéÄÜĮ¦£¬×¢Ņā°ŃĪÕŹµŃéµÄŗĻĄķŠŌŗĶæÉŠŠŠŌµÄĘĄ¼Ū£¬ÄŃ¶Č²»“ó£®


 ĶõŗóŠŪѧ°ø½Ģ²ÄĶźČ«½ā¶ĮĻµĮŠ“š°ø
ĶõŗóŠŪѧ°ø½Ģ²ÄĶźČ«½ā¶ĮĻµĮŠ“š°ø ŗ£µķæĪŹ±ŠĀ×÷Ņµ½š°ń¾ķĻµĮŠ“š°ø
ŗ£µķæĪŹ±ŠĀ×÷Ņµ½š°ń¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | C”¢N”¢OŌŖĖŲµÄµ„ÖŹÓėĒāĘų»ÆŗĻŌ½Ą“Ō½ÄŃ | |
| B£® | Li”¢Na”¢KµÄŃõ»ÆĪļµÄĖ®»ÆĪļµÄ¼īŠŌŅĄ“Ī¼õČõ | |
| C£® | Na”¢Mg”¢AlµÄ¼ņµ„Ąė×ÓµÄŃõ»ÆŠŌŅŌŅĄ“ĪŌöĒæ | |
| D£® | P”¢S”¢ClŌŖĖŲµÄ×īøßÕż¼ŪŅĄ“ĪÉżøߣ¬Ęä¶ŌÓ¦µÄĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌŅĄ“Ī¼õČõ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«Ķ²åČėÅØĻõĖįÖŠ£ŗCu+4H++2NO3?ØTCu2++2NO2”ü+2H2O | |
| B£® | ĻņFeBr2ČÜŅŗÖŠĶØČė¹żĮæĀČĘų£ŗ2Fe2++Cl2ØT2Fe3++2Cl? | |
| C£® | ĻņAl2O3ÖŠ¼ÓČė°±Ė®£ŗAl2O3+2OH?ØT2AlO2?+H2O | |
| D£® | Ģ¼ŗĶÅØĮņĖį¼ÓČČ£ŗC+2H++SO42?ØTH2O+SO2”ü+CO2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČżÕ߶ŌÓ¦µÄŃõ»ÆĪļ¾łĪŖ¼īŠŌŃõ»ÆĪļ | |
| B£® | ČżÕߵĵ„ÖŹ·ÅÖĆŌŚæÕĘųÖŠ¾łÖ»Éś³ÉŃõ»ÆĪļ | |
| C£® | µē½āAlCl3”¢FeCl3”¢CuCl2µÄ»ģŗĻČÜŅŗŹ±Ņõ¼«ÉĻŅĄ“ĪĪö³öCu”¢Fe”¢Al | |
| D£® | ÖʱøAlCl3”¢FeCl3”¢CuCl2¾ł²»ÄܲÉÓĆ½«ČÜŅŗÖ±½ÓÕōøɵķ½·Ø |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ŌŚĖ®ČÜŅŗÖŠ»ņČŪȌדĢ¬ĻĀ¾ł²»µ¼µēµÄ»ÆŗĻĪļ½Š·Ēµē½āÖŹ | |
| B£® | µē½āÖŹ”¢·Ēµē½āÖŹ¶¼Öø»ÆŗĻĪļ¶ųŃŌ£¬µ„ÖŹ²»ŹōÓŚ“Ė·¶³ė | |
| C£® | µē½āÖŹŌŚĖ®ÖŠŅ»¶ØÄܵ¼µē£¬ŌŚĖ®ÖŠµ¼µēµÄ»ÆŗĻĪļŅ»¶ØŹĒµē½āÖŹ | |
| D£® | “æĖ®µÄµ¼µēŠŌŗܲī£¬ĖłŅŌĖ®²»ŹĒµē½āÖŹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
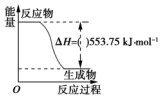 £Ø1£©ŌĖ¶Æ»įÖŠµÄ»š¾ęŅ»°ć²ÉÓƱūĶé£ØC3H8£©ĪŖČ¼ĮĻ£®±ūĶéČČÖµ½Ļøߣ¬ĪŪČ¾½ĻŠ”£¬ŹĒŅ»ÖÖÓÅĮ¼µÄČ¼ĮĻ£®ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ŌĖ¶Æ»įÖŠµÄ»š¾ęŅ»°ć²ÉÓƱūĶé£ØC3H8£©ĪŖČ¼ĮĻ£®±ūĶéČČÖµ½Ļøߣ¬ĪŪČ¾½ĻŠ”£¬ŹĒŅ»ÖÖÓÅĮ¼µÄČ¼ĮĻ£®ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
| »ÆŗĻĪļ | Zn£ØOH£©2 | Fe£ØOH£©2 | Fe£ØOH£©3 |
| Ksp | 1”Į10-17 | 8”Į10-16 | 4”Į10-38 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com