
【题目】某工厂的工业废水中含有大量的Al2(SO4)3、较多的Cu2+和少量的Na+。从工业废水中回收金属铝和金属铜的工艺流程如下图所示(试剂X、Y、Z均过量)。

(1)试剂X为_______,加入试剂X发生的离子方程式是___________试剂Z为___________。
(2)操作②为____________(填实验分离方法)。
(3)溶液2中含有的溶质有__________(填化学式)。
(4)写出操作④的化学反应方程式____________。
(5)金属铜能与浓硫酸在加热的条件下发生反应,产生的气体为_________(填化学式)。
【答案】铝 2Al+3Cu2+=2Al3++3Cu 氨水 过滤 Al2(SO4)3、H2SO4 Al2(SO4)3、H2SO4 SO2
【解析】
某工厂的工业废水中含有大量的Al2(SO4)3、较多的Cu2+和少量的Na+,由流程可知加入X为金属铝,用于置换出铜,溶液1含有Al2(SO4)3、Na2SO4,不溶性物质为过量的Al和Cu的混合物,向不溶性物质中加入试剂Y用于溶解Al,反应产生Al2(SO4)3,而Cu不能发生反应,则为稀H2SO4,溶液2含有Al2(SO4)3、过量H2SO4,由于Al(OH)3是两性物质,能够与过量的强碱NaOH溶液反应产生可溶性物质,因此向①②混合后加入氨水,可生成Al(OH)3沉淀,过滤、洗涤后加热分解生成Al2O3,电解熔融的Al2O3可生成Al,以此解答该题。
根据上述分析可知操作①是过滤,不溶性物质为Cu、Al混合物,操作②是过滤,试剂Y是H2SO4,溶液1含有Al2(SO4)3、Na2SO4,溶液2含有Al2(SO4)3、过量H2SO4,试剂Z是氨水,操作③是过滤,操作④加热分解Al(OH)3,操作⑤是电解。
(1)由以上分析可知X为Al,可用于除去溶液中的Cu2+,反应的离子方程式为:2Al+3Cu2+=2Al3++3Cu;试剂Z为氨水;
(2)操作①②③用于分离固体和液体,为过滤操作;
(3)溶液2中含有的溶质有Al2(SO4)3、H2SO4;
(4)操作④是加热Al(OH)3,Al(OH)3不稳定,受热发生分解反应,化学方程式为:2Al(OH)3![]() 2Al2O3+3H2O;
2Al2O3+3H2O;
(5)金属Cu与浓硫酸混合加热,发生氧化还原反应,产生CuSO4、SO2、H2O,反应方程式为:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O,所以反应产生的气体为SO2。
CuSO4+SO2↑+2H2O,所以反应产生的气体为SO2。


科目:高中化学 来源: 题型:
【题目】抗癌药托瑞米芬的前体K的合成路线如下。

已知:
ⅰ. 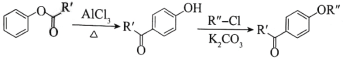
ⅱ.有机物结构可用键线式表示,如(CH3)2NCH2CH3的键线式为![]()
(1)有机物A能与Na2CO3溶液反应产生CO2,其钠盐可用于食品防腐。有机物B能与Na2CO3溶液反应,但不产生CO2;B加氢可得环己醇。A和B反应生成C的化学方程式是___________,反应类型是___________________________。
(2)D中含有的官能团:__________________。
(3)E的结构简式为__________________。
(4)F是一种天然香料,经碱性水解、酸化,得G和J。J经还原可转化为G。J的结构简式为__________________。
(5)M是J的同分异构体,符合下列条件的M的结构简式是__________________。
①包含2个六元环
②M可水解,与NaOH溶液共热时,1 mol M最多消耗2 mol NaOH
(6)推测E和G反应得到K的过程中,反应物LiAlH4和H2O的作用是__________________。
(7)由K合成托瑞米芬的过程:
![]()
托瑞米芬具有反式结构,其结构简式是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,向AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液,观察到的现象是先出现黄色沉淀,最终出现黑色沉淀。已知有关物质的溶度积Ksp(25℃)如表所示:
AgCl | AgI | Ag2S | |
Ksp | 1.8×1010 | 8.3×1017 | 6.3×1050 |
下列叙述错误的是
A.沉淀转化的实质就是沉淀溶解平衡的移动
B.溶解度小的沉淀可以转化为溶解度更小的沉淀
C.AgCl固体分别在等浓度的氯化钾和氯化钙溶液中的溶解度是相同的
D.25℃时,在饱和AgCl、AgI、Ag2S溶液中,所含Ag+的浓度不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2018年10月15日,中国用“长征三号乙”运载火箭成功以“一箭双星”方式发射北斗三号全球组网卫星系统第15、16号卫星,其火箭推进剂为高氯酸铵(NH4ClO4)等。制备NH4ClO4的工艺流程如下:
饱和食盐水![]() NaClO3
NaClO3![]() NaClO4
NaClO4![]() NaClO4
NaClO4![]()
![]() NH4ClO4,下列说法错误的是( )
NH4ClO4,下列说法错误的是( )
A.NH4ClO4属于离子化合物
B.溶解度:NaClO4>NH4ClO4
C.该流程中可循环利用的物质是NH4Cl
D.高氯酸铵中氯元素的化合价为+7价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一项科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO)
(1)向一定物质的量浓度的Cu(NO3)2 和Mn(NO3)2 溶液中加入Na2CO3 溶液,所得沉淀经高温灼烧,可制得CuMn2O4,NO3﹣的空间构型是______________________(用文字描述).
(2)在铜锰氧化物的催化下,CO 被氧化为CO2,HCHO 被氧化为CO2 和H2O.
①根据等电子体原理,CO 分子的结构式为____________.
②H2O 分子中O 原子轨道的杂化类型为____________.
③1mol CO2 中含有的σ键数目为__________________.
(3)H2SeO3的K1和K2分别为2.7×10﹣3和2.5×10﹣8,H2SeO4第一步几乎完全电离,K2为1.2×10﹣2,请根据结构与性质的关系解释:H2SeO3和H2SeO4第一步电离程度大于第二步电离的原因:_______________________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中属于水解反应的是( )
A.CH2=CH2+H2O![]() CH3CH2OH
CH3CH2OH
B.2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
C.CH3CH2Br+NaOH![]() CH3CH2OH+NaBr
CH3CH2OH+NaBr
D.CH3COOH+C2H5OH![]() CH3COOC2H5+H2O
CH3COOC2H5+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物在日常生产生活中用途广泛,利用FeSO4制备还原铁粉的工业流程如下:

实验室中可用FeSO4(用铁粉和稀硫酸反应制得)和NH4HCO3在如下装置模拟上述流程中的“转化”环节。

(1)装置A的名称是________,装置B中盛放的药品是________,NH4HCO3盛放在装置________中。
(2)实验过程中,欲将生成的FeSO4溶液和NH4HCO3溶液混合,操作方法是______________,
发生主要反应的离子方程式为_________。FeSO4溶液要现用现配制的原因是_______,检验久置的FeSO4是否变质的方法是_________________。
(3)干燥过程的主要目的是脱去游离水,该过程中会有少量FeCO3在空气中被氧化为FeOOH,该反应的化学方程式为________,取干燥后的FeCO3样品12.49 g,与炭混合后焙烧,最终得到还原铁粉6.16 g,计算样品中杂质FeOOH的质量:________ g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向AgCl浊液中滴加氨水后可得到澄清溶液,继续滴加浓硝酸后又有沉淀生成。经查资料得知:Ag++ 2NH3·H2O![]() Ag(NH3)2+ 2H2O。下列分析不正确的是
Ag(NH3)2+ 2H2O。下列分析不正确的是
A. 浊液中存在沉淀溶解平衡:AgCl (s)![]() Ag+(aq)+Cl-(aq)
Ag+(aq)+Cl-(aq)
B. 实验可以证明NH3结合Ag+能力比Cl-强
C. 实验表明实验室可用氨水洗涤银镜反应后的试管
D. 由资料信息可推知:加浓硝酸后生成的沉淀为AgCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组以4H++4I-+O2=2I2+2H2O为研究对象,探究影响氧化还原反应因素。
实验 | 气体a | 编号及现象 |
| HCl | Ⅰ.溶液迅速呈黄色 |
SO2 | Ⅱ.溶液较快呈亮黄色 | |
CO2 | Ⅲ.长时间后,溶液呈很浅的黄色 | |
空气 | Ⅳ.长时间后,溶液无明显变化 |
(1)实验Ⅳ的作用是______________。用CCl4萃取Ⅰ、Ⅱ、Ⅲ、Ⅳ的溶液,萃取后下层CCl4的颜色均无明显变化。
(2)取萃取后上层溶液,用淀粉检验:Ⅰ、Ⅲ的溶液变蓝;Ⅱ、Ⅳ的溶液未变蓝。溶液变蓝说明Ⅰ、Ⅲ中生成了______________。
(3)查阅资料:I2易溶于KI溶液。下列实验证实了该结论并解释Ⅰ、Ⅲ的萃取现象。

现象x是______________。
(4)针对Ⅱ中溶液未检出I2的原因,提出三种假设:
假设1:溶液中c(H+)较小。小组同学认为此假设不成立,依据是______________。
假设2:O2只氧化了SO2,化学方程式是______________。
假设3:I2不能在此溶液中存在。
(5)设计下列实验,验证了假设3,并继续探究影响氧化还原反应的因素。
i.取Ⅱ中亮黄色溶液,滴入品红,红色褪去。
ii.取Ⅱ中亮黄色溶液,加热,黄色褪去,经品红检验无SO2。加入酸化的AgNO3溶液,产生大量AgI沉淀,长时间静置,沉淀无明显变化。
iii.取Ⅱ中亮黄色溶液,控制一定电压和时间进行电解,结果如下。
电解时间/min | 溶液 | 阳极 | 阴极 |
t1 | 黄色变浅、有少量SO42- | 检出I2,振荡后消失 | H2 |
| 溶液无色、有大量SO42- | 检出I2,振荡后消失 | H2 |
结合化学反应,解释上表中的现象:______________。
(6)综合实验证据说明影响I-被氧化的因素及对应关系______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com