
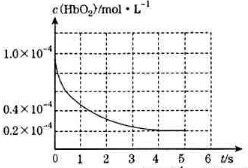
 ��������CO���ڷβ�������ӦCO+HbO2?O2+HbCO��������ȱ������ijѪ����ͨ��CO��O2�Ļ����[c��CO��=1.0��10-4mol/L��c��O2��=9.9��10-4mol/L]����Ѫ�쵰��HbO2Ũ����ʱ��仯������ͼ��ʾ������˵����ȷ���ǣ�������
��������CO���ڷβ�������ӦCO+HbO2?O2+HbCO��������ȱ������ijѪ����ͨ��CO��O2�Ļ����[c��CO��=1.0��10-4mol/L��c��O2��=9.9��10-4mol/L]����Ѫ�쵰��HbO2Ũ����ʱ��仯������ͼ��ʾ������˵����ȷ���ǣ�������| A�� | ��Ӧ��ʼ��4s����HbO2��ʾ��ƽ����Ӧ����Ϊ2��10-4mol/��L•s�� | |
| B�� | ��Ӧ��ƽ��֮ǰ��O2��HbO2�ķ�Ӧ������С | |
| C�� | ��CO�ж����˷����ѹ���������������˻�ѧƽ���ƶ�ԭ�� | |
| D�� | ���¶��·�ӦCO+HbO2?O2+HbCO��ƽ�ⳣ��Ϊ107 |
���� A������v=$\frac{��c}{��t}$�����м��㣻
B��HbO2ת��ΪO2�����Է�Ӧ���Ũ�ȼ��٣�������Ũ�����ӣ�
C����ƽ���ƶ��ĽǶȷ�����
D������ƽ�ⳣ��K=$\frac{c��{O}_{2}��•c��HbCO��}{c��CO��•c��Hb{O}_{2}��}$������ƽ�ⳣ����
��� �⣺A��v=$\frac{��c}{��t}$=$\frac{��1.0-0.2����1{0}^{-4}}{4s}$=2��10-5mol/��L•s������A����
B��HbO2ת��ΪO2�����Է�Ӧ���Ũ�ȼ��٣�������Ũ�����ӣ�������Ӧ���ʼ��٣��淴Ӧ�������ӣ���B����
C��CO�ж��IJ��˷����ѹ�����У�������Ũ������ƽ�������ƶ�����C��ȷ��
D������ƽ�ⳣ��K=$\frac{c��{O}_{2}��•c��HbCO��}{c��CO��•c��Hb{O}_{2}��}$=$\frac{10.7��1{0}^{-4}��0.8��1{0}^{-4}}{0.2��1{0}^{-4}��0.2��1{0}^{-4}}$=214����D����
��ѡC��
���� ���⿼�黯ѧƽ���ƶ��Լ�ƽ�ⳣ���ļ��㣬��Ŀ�Ѷ��еȣ�������ע��ƽ�ⳣ�������弰Ӧ�ã�


 Ӧ����㲦ϵ�д�
Ӧ����㲦ϵ�д� ״Ԫ����ϵ�д�
״Ԫ����ϵ�д� ͬ������ϵ�д�
ͬ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��֬ | B�� | ���� | C�� | ������ | D�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
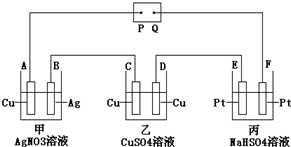
| A�� | P�ǵ�Դ������ | |
| B�� | F���Ϸ����ķ�ӦΪ��4OH--4e-=2H2O+O2�� | |
| C�� | ���ʱ���ס��ҡ��������У���E��F�����⣬����缫���μ��˷�Ӧ | |
| D�� | ͨ��׳���Һ��pH��С���ҳ���Һ��Ũ����������Һ��pH���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
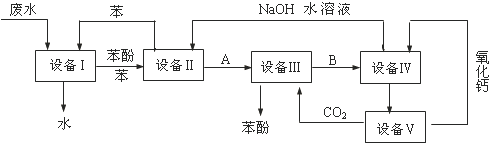
| A�� | ����������豸���н��е��Ƿ�Һ������ʵ������ò��������÷�Һ©������ | |
| B�� | ����������豸���н��е��ǹ��˲�����ʵ������ò����õ��IJ��������У�©�����ձ��������� | |
| C�� | ���豸���з�����Ӧ�Ļ�ѧ����ʽΪ��C6H5ONa+CO2+H2O��C6H5OH+NaHCO3 | |
| D�� | ͼ��ѭ��ʹ�õ�������C6H6��CaO��CO2��NaOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���淴Ӧ�ﵽ��ѧƽ��״̬ʱ�������淴Ӧ���ʾ������� | |
| B�� | ����Ӧ����������Ũ�����ʱ�����淴Ӧһ���Ѵﵽ��ѧƽ�� | |
| C�� | ��ѧ��Ӧ���Ⱦ����˷�Ӧ���ڸ������µ����ת���� | |
| D�� | ��п����Ʒ�Ʋ����������Ʒ������ǰ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
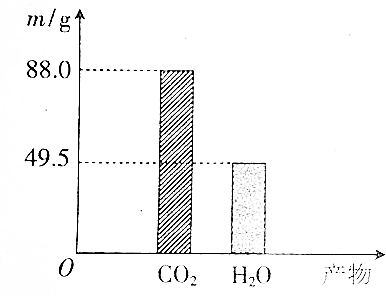
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1.5mol����Fe����������������ȫȼ�գ�ʧȥ4NA������ | |
| B�� | ��25g��������Ϊ60%������ˮ��Һ�У�������ԭ����ΪNA | |
| C�� | 7.8��gNa2S��Na2O2���Ļ�����У����е�������������0.15NA | |
| D�� | ��5��107Pa��500��C������ý�����£�1molN2��3molH2�����ɰ���������Ϊ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
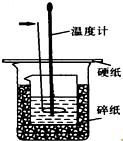 50ml0.50mol•L-1������50mL0.55mol•L-1NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ�����зų��������ɼ����к��ȣ��ش��������⣺
50ml0.50mol•L-1������50mL0.55mol•L-1NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ�����зų��������ɼ����к��ȣ��ش��������⣺�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com