
【题目】随原子序数递增,八种短周期元素(用字母 x 等表示),原子半径的相对大小、最高正价或最低负价的变化如下图所示:

根据判断出的元素回答问题:
(1)g 在周期表中的位置是__________.
(2)d、e、h 的简单离子半径由大到小顺序:_____________(用离子符号表示).
(3)有关 y、z、d 三种元素的说法正确的是__________(填序号).
①最高正价:d>z>y ②简单气态氢化物的稳定性:d>z>y
③非金属性:d>z>y ④单质活泼性:y>z>d
(4)根据g 和h 两种元素填空:
①最高正价氧化物对应水化物的酸性由强到弱的顺序是____________.(用化学式表示)
②g2h2 分子中原子都满足 8 电子结构,试写出其电子式____________.
(5)①试写出x、d、e 形成化合物的水溶液与单质f 反应的化学方程式________________.
②已知化合物A、B 均由 x、d、e、g 四种元素组成,试写出A 和B 反应的离子方程式________________。
【答案】第三周期ⅥA族 Cl->O2->Na+ ②③ HClO4>H2SO4 ![]() 2Al+2NaOH+2H2O=2NaAlO2+3H2↑ H++HSO3-=H2O+SO2↑
2Al+2NaOH+2H2O=2NaAlO2+3H2↑ H++HSO3-=H2O+SO2↑
【解析】
根据元素周期律结合图表可以看出,x位于第一周期,y、z和d位于第二周期,e、f、g和h位于第三周期,从图表的最高正价与最低负价再推出元素所处的族序数,进而推出其元素,分别是H、C、N、O、Na、Al、S和Cl,再结合元素周期律及物质的性质作答。
根据上述分析可知,上述x、y、z、d、e、f、g和h分别是H、C、N、O、Na、Al、S和Cl元素,则:
(1)g为S,在元素周期表的位置是第三周期ⅥA族,
故答案为:第三周期ⅥA族;
(2)电子层数越多,简单离子半径越大,电子层数相同时,核电荷数越小,对应简单离子半径越大。则d、e、h 的简单离子半径由大到小顺序为Cl->O2->Na+,
故答案为:Cl->O2->Na+;
(3)①由于O元素的非金属性很强,其最高正价只能达到+2价,不能达到+6价,①项错误;
②元素的非金属性越强,对应简单气态氢化物的稳定性越大,则稳定性:H2O>NH3>CH4,②项正确;
③同周期从左到右元素非金属性依次增强,则非金属性:O>N>C,③项正确;
④氮气化学键牢固,不活泼,氧气氧化性较强,最活泼,则单质的活泼性:O2> C > N2,④项错误;
答案选②③;
(4)g和h分别为:S和Cl,非金属性Cl>S。
①非金属性越强,则最高正价氧化物对应水化物的酸性越大,故其由强到弱的顺序:HClO4>H2SO4,
故答案为:HClO4>H2SO4;
②g2h2 分子中原子都满足 8 电子结构,根据共价键理论可知,其电子式为:![]() ,
,
故答案为:![]() ;
;
(5)①x、d、e 形成化合物为氢氧化钠,其水溶液与单质铝反应的化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
②由 x、d、e、g 四种元素组成的化合物可以互相反应,则所形成的两种化合物分别是亚硫酸氢钠与硫酸氢钠,在水溶液反应的离子方程式为:H++HSO3-=H2O+SO2↑,
故答案为:H++HSO3-=H2O+SO2↑。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】要使氯化铝溶液中的Al3+完全转化为Al(OH)3沉淀,应选用的最佳试剂是
A. NaOH溶液 B. 稀盐酸 C. 氨水 D. AgNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合理的利用吸收工业产生的废气CO2、NO2、SO2 等可以减少污染,变废为宝。
(1)用CO2可以生产燃料甲醇。
已知:CO2(g)+3H2(g)═CH3OH(g)+H2O(l)△H=﹣akJmol﹣1;
2H2(g)+O2(g)═2H2O(l)△H=﹣b kJmol﹣1;
则表示CH3OH(g)燃烧的热化学方程式为:_______________________。
(2)光气(COCl2)是重要化工原料,常用于聚酯类材料的生产,工业通过Cl2(g)+CO(g)COCl2(g)△H < 0制备。图为实验研究过程中容器内各物质的浓度随时间变化的曲线。回答下列问题:

①0~6min内,反应的平均速率v(Cl2)=___________;
②该反应第一次达平衡时的平衡常数为___________,10min改变的条件是_____________。
(3)利用氨水可以将SO2和NO2吸收,原理如图所示:NO2被吸收的离子方程式是________________________________。
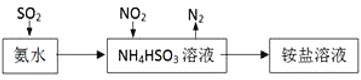
(4)对于2NO(g)+2CO(g)![]() N2(g)+2CO2(g),于1 L的恒容密闭容器中进行反应。下列能说明该反应已经达到平衡状态的是________(填字母代号)。
N2(g)+2CO2(g),于1 L的恒容密闭容器中进行反应。下列能说明该反应已经达到平衡状态的是________(填字母代号)。
A.c(CO)=c(CO2) B.容器中混合气体的密度不变
C.2v(N2)正=v(NO)逆 D.容器中混合气体的平均摩尔质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在难溶电解质AB2的饱和溶液中,c(A2+)=x mol/L,c(B-)=y mol/L,则Ksp(AB2)为( )
A. xy2 B. xy C. 1/2xy D. 4xy2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要0.80 mol·L-1 NaOH溶液 475 mL和0.40 mol·L-1硫酸500 mL。根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是_______(填序号),配制上述溶液还需用到的玻璃仪器是__________________(填仪器名称)。
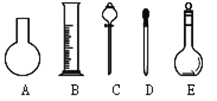
(2)根据计算用托盘天平称取NaOH的质量为______g。其他操作均正确,实验中若还未等溶液冷却就定容了,则所得溶液浓度______0.80 mol·L-1。(填“大于”“等于”或“小于”)
(3)试通过计算,所需质量分数为98%、密度为1.84 g·cm-3的浓硫酸的体积为________mL(计算结果保留一位小数)。
(4)准确称量二水合草酸晶体(H2C2O4·2H2O)m g于锥形瓶中,加适量蒸馏水溶解,滴加2滴______指示剂,用未知浓度的NaOH溶液滴定到终点,终点的颜色变化是______;写出滴定反应的离子方程式:______。通过这种滴定方法,可以准确标定出NaOH溶液的浓度,假设消耗NaOH溶液的体积为VmL,列出计算NaOH准确浓度的式子:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用某工业废铁粉(主要成分为Fe2O3.Fe等)与硫酸反应可制备硫酸亚铁。
(1)Fe元素在周期表中的位置是________写出该废铁粉与硫酸主要反应的离子方程式________________。
(2)FeSO4隔绝空气受热分解生成SO2 SO3 Fe2O3。SO2分子的空间构型为________,其中S原子的杂化轨道类型为________。与SO2互为等电子体的离子与分子分别为________,________(填化学式)
(3)苯酚溶液中滴入Fe3+离子,溶液显________色。1mol苯酚中含有σ键的数目为________。
(4)Fe3O4有反尖晶石结构。某化合物MgxAlyOz与反尖晶石结构相仿,其结构如下图所示,它是由下列A.B方块组成。该化合物的化学式为________.
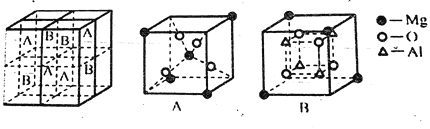
(5)常温条件下,铁的晶体采用如图所示的堆积方式。则这种堆积模型的配位数为________,如果铁的原子半径为0.12nm,阿伏伽德罗常数的值为NA,则此种铁单质的密度表达式为________g/cm3

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】云阳龙缸云端廊桥曾被詟为“世界第一悬挑玻璃景观廊桥”,所用钢化玻璃因其优良的性能广泛应用于日常生活,但由于制作玻璃时里面含有极少量硫化镍,使得钢化玻璃在极限条件下的使用受到限制.
(1)基态硫原子价层电子的轨道表达式(电子排布图)为____________,基态镍原子中核外电子占据最高能层的符号为_____________.
(2)Ni(CO)4常用于制备纯镍,溶于乙醇、CCl4、苯等有机溶剂,为___________晶体,Ni(CO)4空间构型与甲烷相同,中心原子的杂化轨道类型为___________,写出与配体互为等电子体的阴离子__________________________________________________________(任写一种).
(3)与硫同族的硒元素有两种常见的二元含氧酸,请比较它们酸性强弱 > (填化学式)______,理由是_______________________________________________________________.
(4)H2S的键角__________(填“大于”“小于””等于”)H2O的键角,请从电负性的角度说明理由___________________________________________________.
(5)NiO与NaCl的晶胞结构相似,如图所示,阴离子采取面心立方堆积,阳离子填充在位于阴离子构成的空隙中,已知Ni2+半径为69nm,O2-半径为140nm,阿伏伽德罗常数为NA,NiO晶体的密度为_________g/cm3(只列出计算式).

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下硫酸亚铁发生反应2FeSO4 ![]() Fe2O3+SO2↑+SO3↑,若将生成的气体通入氯化钡溶液中,得到的沉淀是
Fe2O3+SO2↑+SO3↑,若将生成的气体通入氯化钡溶液中,得到的沉淀是
A. BaS B. BaSO3 C. BaSO4 D. BaSO3和BaSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2的转换在生产、生活中具有重要的应用。
Ⅰ.CO2的低碳转型对抵御气候变化具有重要意义。
(1)海洋是地球上碳元素的最大“吸收池”。
①溶于海水中的CO2主要以四种无机碳形式存在,除CO2、H2CO3两种分子外,还有两种离子的化学式为____________。
②在海洋碳循环中,可通过下图所示的途径固碳。写出钙化作用的离子方程式:_____________。
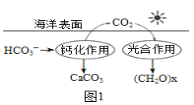
(2)将CO2与金属钠组合设计成Na-CO2电池,很容易实现可逆的充、放电反应,该电池反应为4Na+3CO2 ![]() 2Na2CO3+C。放电时,在正极得电子的物质为______;充电时,阳极的反应式为_____。
2Na2CO3+C。放电时,在正极得电子的物质为______;充电时,阳极的反应式为_____。
Ⅱ.环境中的有害物质常通过转化为CO2来降低污染。
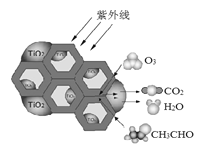
(3)TiO2是一种性能优良的半导体光催化剂,能有效地将有机污染物转化为CO2等小分子物质。下图为在TiO2的催化下,O3降解CH3CHO的示意图,则该反应的化学方程式为____。
(4)用新型钛基纳米PbO2作电极可将苯、酚类等降解为CO2 和H2O。该电极可通过下面过程制备:将钛基板用丙酮浸泡后再用水冲洗,在钛板上镀上一层铝膜。用它做阳极在草酸溶液中电解,一段时间后,铝被氧化为氧化铝并同时形成孔洞。再用Pb(NO3)2溶液处理得纳米PbO2,除去多余的氧化铝,获得钛基纳米PbO2电极。
①用丙酮浸泡的目的是______。
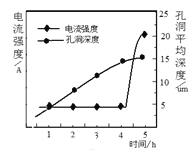
②电解时,电流强度和基板孔洞深度随时间变化如图所示,氧化的终点电流突然增加的原因是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com